
Präklinische "Volumentherapie"
Präklinische Volumen- bzw. Flüssigkeits-Therapie beim Polytrauma-Patienten
Kommentar zu vier Arbeiten aus der Arbeitsgruppe Hußmann (Essen), im Folgenden nach dem Erscheinungsjahr benannt: 2011, 2012, 2013 und 2015
Herr Dr. B. Hußmann, Klinik für Unfallchirurgie, Universitätsklinikum Essen (jetzt im Alfried Krupp Krankenhaus Essen-Rüttenscheid tätig), war leider nicht zu einer Stellungnahme bereit.
Welche Infusionslösungen werden eingesetzt?
Flüssigkeitstherapie: Was, wann und wie viel?
Zitat aus einem Physioklin-Beitrag aus 2006: „Es ist erfreulich, dass alle drei deutschsprachigen Anästhesiologie-Zeitschriften fast zeitgleich (April - Juni 2006) das Thema „Perioperatives Flüssigkeitsmanagement“, „Volumenersatztherapie“ und „Flüssigkeitsmanagement“ aufgreifen. Frustrierend ist, dass die entscheidende Frage, nämlich das Was, neben dem Wann und Wie viel kaum behandelt wird. Um das Fazit vorwegzunehmen: Es ergibt keinen Sinn, das Wann und Wie viel zu behandeln ohne primär über das Was entschieden zu haben.“
Das gleiche Problem wiederholt sich jetzt in den 4 Arbeiten der Gruppe Hußmann. Hier wird über das präklinisch applizierte Infusions-Volumen berichtet, eine Differenzierung zwischen Kristalloiden, Kolloiden und hyperosmolalen Lösungen wird nicht vorgenommen. Unter Limitations wird 2015 (falsch) berichtet:
„As a rule, Ringer´s solution or 0.9 % NaCl are used as crystalloid solutions, HAES1 is used as colloidal solution, and HyperHAES1 as a hyperoncotic solution”, gemeint ist eine isoonkotische hypertone bzw. hyperosmolale Lösung. Der gleiche Fehler findet sich 2011 (hyperonkotische Lösungen) und 2013 (Tab. 2 hyperoncotic solutions).
Natürlich hat das Was einen erheblichen bis entscheidenden Einfluss auf das Ergebnis:
In 2011 werden Kristalloide, Kolloide und hyperosmolale Lösungen ohne Angabe der Verteilung eingesetzt, in 2012 nur Kristalloide und Kolloide, in 2013 alle drei Lösungen mit einer Verteilung von 65 bzw. 89 % Kolloide und 10,3 bzw. 24,1 % hyperosmolale Lösungen, und in 2015 nur Kristalloide und Kolloide mit einem Kolloid-Anteil von 47 bzw. 53 %.
Wenn in 2013 10,3 % der low-volume Patienten hyperosmolale Lösungen erhalten haben, dann hat dies sicher einen Einfluss auf das Ergebnis, insbesondere wenn 24,1 % der high-volume Patienten diese problematischen hyperosmolalen Lösungen erhalten haben, von denen aktuell abgeraten wird.
Auch ein Unterschied von 65 bzw. 89 % der Patienten, die kolloidale Lösungen erhalten haben, dürfte einen Einfluss auf das Ergebnis haben.
Sind die verwendeten Infusionslösungen heute veraltet bis kontraindiziert?
Die Daten wurden zu ähnlichen Zeitpunkten erhoben, immer beginnend im Jahre 1993 und endend zwischen 2007 und 2010. Abgesehen von den hyperosmolalen Lösungen wurden in diesem Zeitraum Ringer-Laktat-Lösungen (vermutlich nicht Ringer's solution, s.o.) und 0,9 % NaCl verwendet, der Abschied von 0,9 % NaCl wurde schon 2013 feierlich begangen. Das bedeutet, dass die erhobenen Daten über das zugeführte Volumen kaum verwertbar sind, weil sich die heute allgemein verwendeten balancierten (physiologischen) kristalloiden und/oder kolloidalen Lösungen deutlich von den damals verwendeten Lösungen unterscheiden. Sie wären heute kontraindiziert.
Grobe Nachlässigkeiten in den 4 Arbeiten
2011, 2012, 2013, 2015
Hb-Konzentration in mg/dl
2012
Herzfrequenz in Sekunden, Atemfrequenz ohne Einheit, BE ohne Einheit
2013
Herzfrequenz in Sekunden, BE ohne Einheit, Thrombozytenzahl / nl - z.B. 192.887,0 / 73.574,0 (unsinnige Zahlen, Bruchteile von Thrombos?)
2015
BE ohne Einheit, Thrombozyten n / nl - z.B. 219.326,53 (unsinnige Zahlen, Bruchteile von Thrombos?)
[Möglichkeiten zur Angabe der Thrombozytenzahl:
~ 300 x 109 / l = ~ 300 x 106 / ml = ~ 300 x 103 / µl = ~ 300 / nl]
Ungereimtheiten
2011
Gibt es einen Sinn, zusätzlich ca. 21 min aufzuwenden, um weitere ca. 3,7 Liter Infusionsvolumen zu infundieren?
2011 - 2015
Spielt es keine Rolle, dass die Patienten, die mehr Volumen erhalten hatten, auch präklinisch bereits signifikant häufiger Katecholamine benötigt haben?
Welche Indikation wird für die Transfusion von 5 - 15 EK's genannt, wenn die cHb (g/dl) bei Aufnahme, von wenigen Ausnahmen abgesehen, "harmlose" Werte aufweist?
Welche entscheidenden Veränderungen über die ersten 24 Stunden haben die folgenden Werte erfahren: cHb (g/dl), BE (mmol/l) und Laktat-Konzentration (Lactat-Clearance)? Die niedrigste cHb bei Aufnahme beträgt 7,2 g/dl (2012) und erfordert 6,9 EK's? Ist es den Autoren klar, dass EK's einen optimalen Volumeneffekt besitzen?
Einzeldaten in den verschiedenen Gruppen
Die Einzeldaten sind in der folgenden Tabelle aufgeführt.
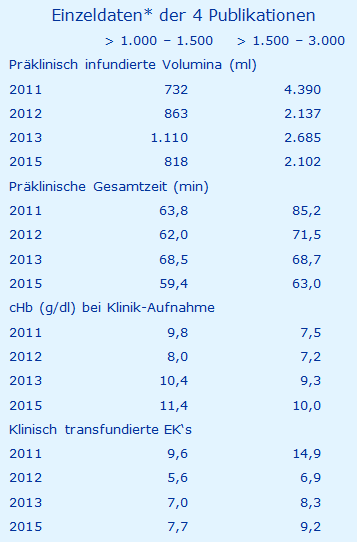
* Die nach den infundierten Volumina (ml) gebildeten Gruppen wurden auf 2 reduziert, sie waren 2011 < 1.000 vs. > 3.000; 2012 Low vs. high; 2013 < 1.500 vs. > 1.501 und 2015 0 - 1000 vs. > 1.500 (die Gruppe 1.000 bis 1.500 wurde hier ohne Angabe von Gründen gestrichen); für die in 2011 angegebenen Daten für „Abdominal“ vs. „Becken“ wurde ein Mittelwert gebildet, da sie sich kaum unterschieden; Zahlen mit 2 Stellen nach dem Komma wurden aufgerundet.
Interpretation
In den 4 Arbeiten werden retrospektiv erhobene Korrelationen in Kausalitäten umgemünzt und die bekannten Prognose-Indikatoren vollständig ignoriert. Ein schwer verletzter Polytrauma-Patient weist nämlich einige Korrelationen auf, die die Mortalität sehr gut prognostizieren können (Abbildungen mit einer Ausnahme aus Zander R: Flüssigkeitstherapie, 2. erw., korr. Aufl. 2020; dort findet sich auch die jeweils angegebene Literatur.
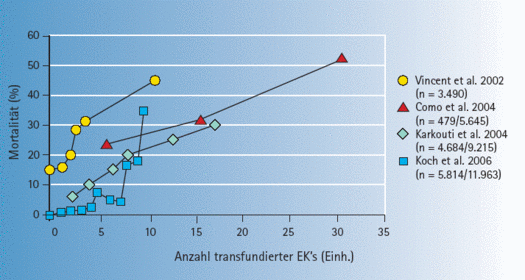
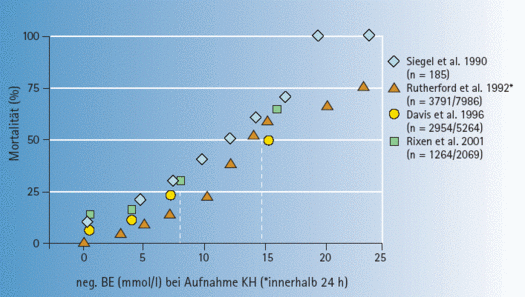
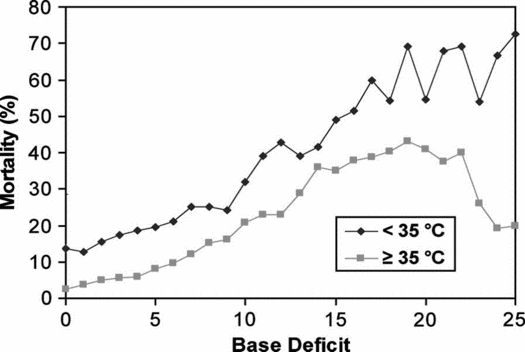
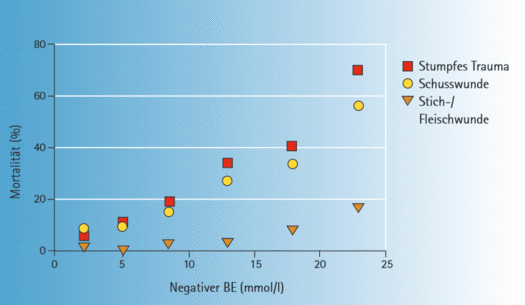
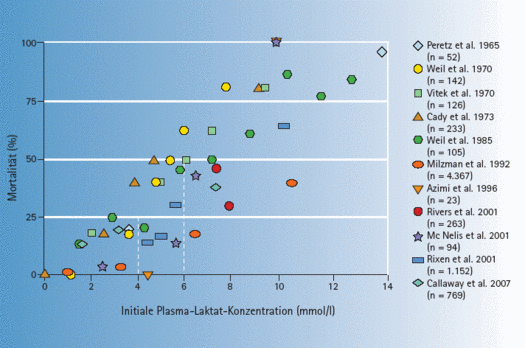
Die folgenden Zitate (rot) sind höchst problematisch
Es besteht ein eindeutiger Unterschied zwischen einer retrospektiv erhobenen Korrelation und einer Kausalität.
Zitat: “Finally, we only conducted a retrospective analysis, so only associations (not causalities) can be ascribed to the given data” (2013).
Diese eindeutige Aussage wird von den Autoren nicht durchgängig verfolgt:
2011
Die moderate Flüssigkeitssubstitution (< 1000 ml) führt zu einer Reduktion transfundierter Blutprodukte und vermindert hierdurch zusätzlich die Infektionsgefahr.
Ein schlechteres Outcome kann auch über die steigende Volumenmenge erklärt werden.
2012
For the first time, a tendency was shown that excessive prehospital fluid replacement in children leads to a worse clinical course with higher mortality…..
2013
One remarkable finding of this study is that a higher replacement volume was related to a significantly higher mortality rate. It can be assumed…. that an increased prehospital replacement volume is responsible for the higher mortality rate after trauma…
2015
Excessive prehospital fluid replacement is able to lead in an increased mortality rate in patients with solid abdominal organ injury.
Für Leser, die gerne der Verführung folgen, Korrelationen als Kausalitäten zu interpretieren, ist am Ende dieses Beitrages ein Anhang angefügt.
Was bleibt – zu Recht
Eine Empfehlung der Interdisziplinären Arbeitsgruppe Schock der DIVI aus dem Jahre 2005 zur permissiven Hypotension:
„Dagegen ist nach perforierendem oder penetrierendem Trauma mit zunächst unstillbarer starker Blutung in die großen Körperhöhlen Thorax und Abdomen anfangs die zurückhaltende Volumenzufuhr mit permissiver Hypotonie geboten, um den mit dem Blutdruck steigenden Volumenverlust sowie jeden Zeitverzug bis zur chirurgischen Versorgung zu vermeiden. Zielwerte für den Blutdruck sind nicht bekannt und insbesondere von vorbestehenden Erkrankungen (z. B. einer Hypertonie) abhängig. In Anlehnung an das Vorgehen bei extrakorporaler Zirkulation kann ein MAP von 50 mmHg bzw. ein SAP von 70 - 80 mmHg als ausreichend gelten. Nach der chirurgischen Blutstillung ist unverzüglich für die suffiziente Auffüllung des Kreislaufs zu sorgen.“
Fazit
In 4 extrem nachlässig publizierten Arbeiten aus einer Essener Arbeitsgruppe wird über die präklinische "Volumentherapie" berichtet, deren Ergebnisse aus folgenden Gründen nicht verwertbar sind: Die Reduktion auf die Größe des infundierten präklinischen Volumens allein ist nicht statthaft, die damals verwendeten Lösungen sind nicht mehr aktuell und wären heute kontraindiziert, retrospektiv erhobene Korrelationen dürfen nicht als Kausalitäten interpretiert werden.
Literatur
2011
Hußmann B, Taeger G, Lefering R et al.
Letalität und Outcome beim Mehrfachverletzten nach schwerem Abdominal- und Beckentrauma
Unfallchirurg 2011; 114: 705 - 712
2012
Hussmann B, Lefering R, Kauther MD et al.
Influence of prehospital volume replacement on outcome in polytraumatized children
Crit Care 2012; 16: R201
2013
Hussmann B, Lefering R, Waydhas C et al.
Does increased prehospital replacement volume lead to a poor clinical course and an increased mortality? A matched-pair analysis of 1896 patients of the Trauma Registry of the German Society for Trauma Surgery who were managed by an emergency doctor at the accident site
Injury 2013; 44: 611 - 617
2015
Heuer M, Hussmann B, Lefering R et al.
Prehospital fluid management of abdominal organ trauma patients-a matched pair analysis
Langenbecks Arch Surg 2015; 400: 371 379
Adams HA, Baumann G, Cascorbi I, Ebener C, Emmel M, Geiger S, Janssens U, Klima U, Klippe HJ, Knoefel WT, Marx G, Müller-Werdan U, Pape HC, Piek J, Prange H, Roesner D, Roth B, Schürholz T, Standl T, Teske W, Vogt PM, Werner GS, Windolf J, Zander R, Zerkowski HR und die IAG Schock
Zur Diagnostik und Therapie der Schockformen – Empfehlungen der Interdisziplinären Arbeitsgruppe Schock der DIVI
Teil II - Hypovolämischer Schock
Anästh Intensivmed 2005; 46: 111 - 124
Martin RS, Kilgo PD, Miller PR, Hoth JJ, Meredith JW, Chang MC
Injury-associated hypothermia: an analysis of the 2004 National Trauma Data Bank
Shock 2005; 24: 114 - 118
Anhang
Die Süddeutsche Zeitung (Werner Bartens) berichtet am 19. Juni 2015 unter der Überschrift „Zu süß, um wahr zu sein“ Folgendes:
„Manchmal macht die Wissenschaft herrliche Versprechen. Was für verlockende Aussichten wurden im Fachmagazin Heart (online) in dieser Woche verbreitet!
Wer regelmäßig Schokolade isst, senkt demnach sein Risiko, einen Infarkt oder Schlaganfall zu erleiden, beträchtlich.
Es handelt sich um eine Beobachtungsstudie. Wer gerne Schokolade isst, wird seltener krank, besagt sie simpel. Ein kausaler Zusammenhang ist damit noch längst nicht belegt, nur eine Korrelation.
Die Autoren erwähnen denn auch, dass ihre Schokoladenliebhaber nicht nur gerne Schokolade aßen, sondern im Mittel auch jünger, schlanker und körperlich aktiver waren. Zudem litten sie seltener an Diabestes, hatten einen niedrigeren Blutdruck, und der Spiegel ihrer Entzündungswerte im Blut lag niedriger.“
