
Abschied von 0,9 % NaCl
Es wird höchste Zeit, dass die Verwendung von 0,9 % NaCl als Infusionslösung
→ seit 1970 „neither „normal“ nor physiological“ [10]
→ seit 2003 „(ab)normal saline“ [7]
unterbleibt, weil die Nebenwirkungen zu schwerwiegend sind:
- Renale Vasokonstriktion mit Abnahme der GFR und damit der Diurese
- Suppression der Plasma-Renin-Aktivität mit Abfall des Blutdrucks
- Hyperchlorämie mit Hyperhydratation
- Hyperchlorämische Azidose
- Hypernatriämie
Damit sollte die Indikation für 10 bis 200 Millionen Liter NaCl 0,9 % (UK, USA) entfallen [3].
Verteilung
Wie alle kristalloiden Lösungen verteilt sich NaCl 0,9 % so, dass nur ca. 20 % im intravasalen Flüssigkeitsvolumen (IVFV) verbleiben, während die restlichen 80 % sehr schnell in das extrazelluläre Flüssigkeitsvolumen (ECFV) diffundieren und dort eine Hyperhydratation bewirken. Dies kann mit einer großen Zahl von Literaturdaten belegt werden, hier mit 6 Literaturstellen 0,9 % NaCl betreffend, Kristalloide intravasal, die einen Mittelwert von 23 % für das IVFV ergeben.
Für hypotone Lösungen wie Ringer-Laktat wurde kürzlich experimentell nachgewiesen, dass der Wert von 20 % erwartungsgemäß leicht unterschritten wird, weil freies Wasser dem osmotischen Gradienten folgend zusätzlich in das ICFV diffundieren muss.
Änderung des Elektrolytmusters
Erhält ein Patient von 75 kg KG mit einem ECFV von 15 l eine Infusion von 5 l NaCl 0,9 % (je 154 mmol/l Na bzw. Cl), dann steigt die Natrium-Konzentration nur um 3 mmol//l von 142 auf 145 mmol/l an, während die Chlorid-Konzentration immerhin von 103 auf 116 mmol/l ansteigt. Allein diese Bilanz macht deutlich, dass eine Hyperchlorämie (korrekte Bezeichnung eigentlich Hyperchloridämie) sehr viel eher zu erwarten ist als eine Hypernatriämie.
Dass eine intraoperative Gabe von 5,1 bis 7,0 l NaCl 0,9 % innerhalb von 2 bis 5 Stunden bei gleichzeitiger Urinausscheidung von 0,6 bis 1,2 l und Dilution des ECFV von 35 bis 37 % realistisch ist, wird durch die Literatur belegt [2, 9, 11]. Dabei stimmt die Vorhersage der Elektrolytkonzentrationen, wie hier beschrieben, sehr gut mit den erhobenen Messwerten überein.
Hyperchlorämie
Im Tierexperiment verursacht eine Hyperchlorämie, (nicht die Hypernatriämie) von 103 auf 115 mmol/l, also vergleichbar der Zufuhr von 5 l NaCl 0,9 %:
Einerseits eine spezifisch renale Vasokonstriktion mit Zunahme des renalen Gefäßwiderstandes um 35 % und konsekutive Abnahme der GFR um 20 % und somit Abnahme der Diurese.
Andererseits eine Suppression der Plasma-Renin-Aktivität mit konsekutivem Abfall des Blutdruckes. Dies wird belegt mit 4 Literaturstellen [13].
Am Menschen verursacht eine Infusion von 2 l einer 0,9 % NaCl-Lösung am Probanden einen Abfall des Hämatokrits um 10 % (nur 20 % verbleiben im IVFV), eine Hyperchlorämie von „harmlosen“ 108 mmol/l und trotzdem eine Suppression des Renin-Aldosteron-Systems auf 60 % für die Dauer von 2 Tagen [5].
Hyperchlorämie und Nierenfunktion
Nach Infusion von 2 l NaCl 0,9 % innerhalb von 2 Stunden bei gesunden Erwachsenen wurde aktuell eine signifikante Abnahme der Blutfluss-Geschwindigkeit in der Nierenarterie bis zu 13 % und der Durchblutung des Nierencortex um 11,7 % demonstriert, wobei die Chlorid-Konzentration nur von 103 auf harmlose 108,5 mmol/l anstieg [3].
Die klinischen Vorteile einer Restriktion hyperchlorämischer Lösungen lassen sich eindeutig nachweisen: Wird nach Einschluss von 760 ICU-Patienten ein vergleichbares zweites Kollektiv von 773 Patienten zeitlich versetzt über 6 Monate konsequent nur noch mit normochlorämischen Lösungen versorgt, geht das akute Nierenversagen (AKI) von 14 auf 8,4 % zurück, ebenso die notwendige Nierenersatztherapie (RRT) von 10 auf 6,3 % [12].
Nachtrag (15.03.2015)
Eine Meta-Analyse anhand von 6.253 Patienten aus 21 Studien hat ergeben, dass der Einsatz von Infusionslösungen mit einer Chloridkonzentration von 111 bis 154 mmol/l im Vergleich zu solchen mit 111 oder weniger mmol/l zwar zu keiner Erhöhung der Mortalität führt, neben anderen Effekten aber sehr wohl das Risiko einer akuten Nierenschädigung signifikant erhöht. Das bedeutet, dass das Thema Hyperchlorämie die Infusionstherapie der kommenden Jahre sehr stark dominieren wird, zumal 0,9 % NaCl in vielen Studien als „Kontroll-Flüssigkeit“ verwandt wurde.
Krajewski ML, Raghunathan K, Paluszkiewicz SM et al:
Meta-analysis of high- versus low-chloride content in perioperative and critical care fluid resuscitation. Br J Surg 2015; 102: 24 - 36 (Summary)
Renale Korrektur einer hyperchlorämen Hyperhydratation?
Sollte man nicht erwarten, dass diese hyperchloräme Hyperhydratation mit entsprechender Zunahme des Körpergewichts relativ schnell durch die Niere im Sinne einer Flüssigkeits-Elimination, also Diurese, kompensiert wird? Dies trifft offensichtlich nicht zu.
Bei exzessiver Flüssigkeitstherapie, gemeint sind 5 – 50 l pro Tag, mit hyperchlorämischen Lösungen (0,9 % NaCl, Ringer-Laktat) ist die maximale tägliche Urinausscheidung auf ca. 3 l limitiert, wie sich aus entsprechenden Literaturdaten ergibt:
Der Mittelwert von 9 Untersuchungsreihen beträgt 3,1 ± 0,7 l/d (7 Literaturstellen von 1979 bis 2000) [13].
Aber auch 2009 kann diese, renal nicht kompensierte Hyperhydratation noch beobachtet werden: Trotz exzessiver Flüssigkeitszufuhr von 34 l über 5 Tage beträgt die mittlere Urin-Ausscheidung im gleichen Zeitraum nur 3,0 l, wie am Beispiel eines Patienten unter Ketoacidose demonstriert wurde.
Folgen einer Hyperhydratation
Vor den Folgen einer aggressiven Kristalloid-basierten Flüssigkeitstherapie wird ausdrücklich gewarnt: Kardiale und pulmonale Komplikationen, gastrointestinale Fehlfunktionen, Gerinnungsstörungen usw. [4]. Dies gilt im Besonderen für Kinder, weil hier eine positive Flüssigkeitsbilanz (fluid overload) negative Auswirkungen auf die Organfunktion und das Outcome hat [1].
Hypernatriämie
Die Infusion größerer Volumina von 0,9 % NaCl führt wie gezeigt auch zu einer Hypernatriämie, die durchaus problematisch werden kann, wie in einer Publikation gezeigt [6]. Danach besteht ein Zusammenhang zwischen der Natrium-Konzentration bei Aufnahme auf der Intensivstation (ITS) und der Mortalität auf der ITS bzw. der Mortalität im Krankenhaus (KH). Die über einen Zeitraum von 10 Jahren erhobenen Befunde von 151.486 Intensiv-Patienten von 77 medizinischen bzw. chirurgischen ITS sind in der folgenden Abbildung dargestellt.
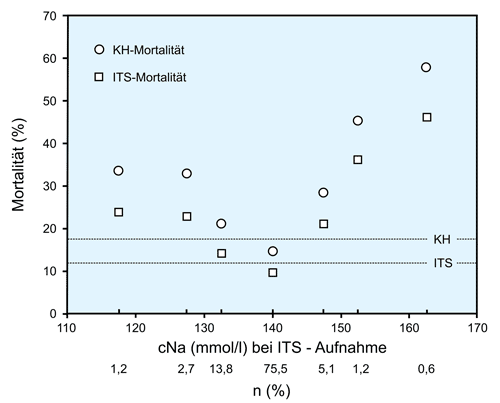
Bei immerhin ~ 7.600 Patienten (5 %), also ~ 760 pro Jahr, mit einem Anstieg der Na-Konzentration um ~ 7 mmol/l verdoppelte sich sowohl die IST- als auch die KH-Mortalität.
Dilutions-Azidose
Erhält der bereits erwähnte Patient (75 kg KG, ECFV 15 l) eine 5 l-Infusion von 0,9 % NaCl ohne Bikarbonat, dann wird die HCO3-Konzentration des Plasmas und des ECFV von normal 24 auf 18 mmol/l verdünnt (diluiert) und der pH fällt von 7,40 (bei pCO2 40 mmHg) auf 7,27.
Dies entspricht einem Basendefizit von 8,5 mmol/l (neg. BE) und charakterisiert eine hyperchlorämische Azidose. Wichtig ist hier der erneute Hinweis, dass je nach verwandter Infusionslösung iatrogene hyper- und hypo-chlorämische Azidosen und Alkalosen erzeugt werden können: Münchner Entgleisungen
Sonderfall Pädiatrie
Mit einem klassischen Beispiel aus der Kinder-Anästhesie wird die Problematik einer Hyperhydratation nach vermuteter Gabe von NaCl 0,9 % beschrieben, die Daten wurden 2011 freundlicherweise von Herrn Prof. Dr. R. Sümpelmann (Medizinische Hochschule Hannover) zur Verfügung gestellt.
Ein Frühgeborenes wird von extern mit einem KG von 790 g eingeliefert, das folgende Bild zeigt den Patienten mit den (kaum lesbaren) Daten der Diagnostik bei Aufnahme.
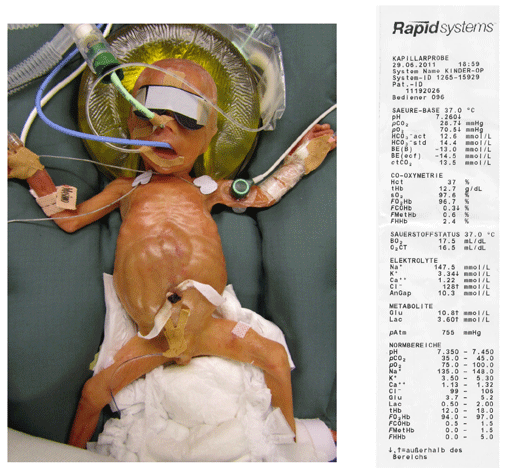
Die gesonderte Auswertung zeigt die folgende Tabelle:
Unterstellt, dass das Kind (KG 590 g) mit 200 ml NaCl 0,9 % behandelt wurde, iterativ ermittelt aus dem Anstieg der Natrium-Konzentration, zeigen die gemessenen Werte von Chlorid und HCO3 eine optimale Übereinstimmung. Die gleiche Übereinstimmung ergibt sich dann auch unter Verwendung des gemessenen pCO2 für den pH- und BE-Wert.
Somit zeigt das Kind anhand von 5 optimal übereinstimmenden Werten das klassische Bild einer iatrogenen hypernatriämischen, hyperchlorämischen Dilutions-Azidose nach Infusion von 200 ml 0,9 % NaCl.
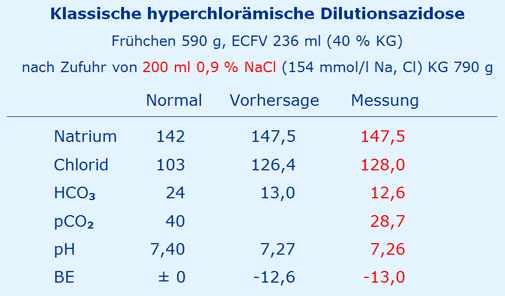
Dies wäre mit einer balancierten Lösung für die Pädiatrie zu verhindern gewesen [8].
Zusammenfassung
Die Infusion von NaCl 0,9% führt zu schwerwiegenden Nebenwirkungen, nämlich einer
- renalen Vasokonstriktion mit Abnahme der GFR und damit der Diurese mit der Gefahr einer Nierenschädigung,
- Suppression der Plasma-Renin-Aktivität mit Abfall des Blutdrucks,
- Hyperchlorämie mit Hyperhydratation und ihren negativen Folgen,
- hyperchlorämischen Azidose sowie
- Hypernatriämie.
Diese Gefahr wird heute mit dem Einsatz so genannter balancierter ISO-Lösungen vermieden, Lösungen mit plasmaadaptierter, also physiologischer Zusammensetzung.
Diese physiologische Zusammensetzung verhindert - und korrigiert partiell - alle iatrogenen Störungen im Elektrolyt- (Na, K, Ca, Cl), Osmolalitäts-, Säure-Basen- und Gerinnungs-Status (Entscheidungshilfe Infusionslösungen).
Literatur
- Arikan AA, Zappitelli, M, Goldstein SL et al.:
Fluid overload is associated with impaired oxygenation and morbidity in critically ill children.
Pediatr Crit Care Med 2012; 13: 253-258 - Bruegger D, Jacob M, Scheingraber S et al.:
Changes in acid-base balance following bolus infusion of 20% albumin solution in humans.
Intensive Care Med 2005; 31: 1123-1127 - Chowdhury AH, Cox EF, Francis ST et al.:
A randomized, controlled, double-blind crossover study on the effects of 2-L infusions of 0.9% saline and Plasma-Lyte 148 on renal blood flow velocity and renal cortical tissue perfusion in healthy volunteers.
Ann Surg 2012: 256:18-24 - Cotton BA, Guy JS, Morris Jr JA et al.:
The cellular, metabolic, and systemic consequences of aggressive fluid resuscitation strategies.
Shock 2006; 26:115-121 - Drummer C, Gerzer R, Heer M et al.:
Effects of an acute saline infusion in fluid and electrolyte metabolism in humans.
Am J Physiol 1992; 262: F744-F754 - Funk GC, Lindner G, Druml W et al.:
Incidence and prognosis of dysnatremias present on ICU admission.
Intensive Care Med. 2010; 36: 304-311 - Reid F, Lobo DN, Williams RN et al.:
(Ab)normal saline and physiological Hartmann’s solution: A randomized double-blind crossover study.
Clin Sci 2003; 104: 17-24 - Sümpelmann R, Mader T, Dennhardt N et al.:
A novel isotonic balanced electrolyte solution with 1% glucose for intraoperative fluid therapy in neonates: results of a prospective multicentre observational postauthorisation safety study (PASS).
Paediatr Anaesth. 2011; 21: 1114-1118 - Takil A, Eti Z, Irmak P et al.:
Early postoperative respiratory acidosis after large intravascular volume infusion of lactated Ringer’s solution during major spine surgery.
Anesth Analg 2002; 95: 294-298 - Wakim KG: ”Normal” 0.9 % salt solution is neither “normal” nor physiological.
JAMA 1970; 214: 1710 - Waters JH, Gottlieb A, Schönwald P et al.:
Normal saline versus lactated Ringer’s solution for intraoperative fluid management in patients undergoing abdominal aortic aneurysm repair: An outcome study.
Anesth Analg 2001; 93: 817-822 - Yunos NM, Balloon R, Hegarty C et al.:
Association between a chloride-liberal vs chloride-restrictive intravenous fluid administration strategy and kidney injury in critically ill adults.
JAMA 2012; 308: 1566-1572 - Zander R: Flüssigkeitstherapie, 2. erweiterte (korrigierte) Auflage, 2020
