
Hypernatriämie – insbesondere bei Antibiotika-Therapie
Ein Beitrag von Rolf Zander (Mainz) unter Mitarbeit von Barbara Reistle (Stuttgart)*
Einleitung: Hypernatriämie versus isolierte Hypernatriämie
Die häufigste Ursache einer einfachen iatrogenen Hypernatriämie wäre die Gabe von NaCl, meist in Form von 0,9 %iger Lösung, der so genannten physiologischen Kochsalzlösung. Diese Hypernatriämie ist automatisch mit einer entsprechenden Hyperchlorämie (eigentlich Hyperchloridämie) verbunden. Entsprechend bedeutet allerdings, dass die Hyperchlorämie deutlicher ausgeprägt ist als die Hypernatriämie: 1 l einer 0,9 % NaCl (je 154 mmol/l Na und Cl) erhöht bei einem Patienten von 75 kg KG mit einem Extracellularvolumen (ECV) von 15 l die Plasma-Natrium-Konzentration nur um 0,8 mmol/l, während die Chloridkonzentration immerhin um 3,2 mmol/l ansteigt. Auch dies dürfte ein Grund dafür sein, die Gabe von 0,9 % NaCl heute zu vermeiden, wie im Beitrag Abschied von 0,9 % NaCl ausführlich begründet.
Im Gegensatz hierzu soll mit der Bezeichnung „isolierte Hypernatriämie“ ein Zustand beschrieben werden, bei dem im Plasma des Patienten, und damit im gesamten ECV, die Natrium-Konzentration allein über den Normalwert hinaus (142 mmol/l) erhöht ist, ohne dass andere Elektrolyte, insbesondere Chlorid (103 mmol/l), ebenfalls erhöht wären.
Folgt man den Anfragen bei Physioklin, dann ist diese Störung nicht gerade selten. Immer sehr spekulativ wurde hier und auf Veranstaltungen regelmäßig der Einsatz von Antibiotika als Ursache vermutet. Da es jetzt gelungen ist, den Natrium-Gehalt der Antibiotika exakt zu beschreiben, wird dieser Beitrag veröffentlicht.
Mögliche Ursachen einer isolierten Hypernatriämie
Diese Form der Hypernatriämie – ohne Hyperchlorämie – kommt immer dann zustande, wenn das Natrium (Kation) in Verbindung mit einem Nicht-Chlorid-Anion zugeführt wird, das in den Intrazellularraum (ICV) diffundiert, im Stoffwechsel metabolisiert oder über Lunge (CO2) und Niere (H2O) eliminiert wird.
Als Beispiele können genannt werden:
- Natrium-Citrat, -Azetat, -Laktat oder -Aspartat
- Natrium-Bikarbonat
- Antibiotika-Natrium
Isolierte Hypernatriämie nach Plasma-Transfusion
Bei der Verwendung von Tri-Natrium-Citrat als Antikoagulans landet der überwiegende Teil des zugeführten Citrats (ca. 95 %) und damit auch des Natriums im Plasma. Für das Plasma wurden die Natrium-Konzentrationen bereits vorhergesagt, nämlich für FFP (fresh frozen plasma) aus der Blutspende eine Natrium-Konzentration von 170,8 mmol/l und beim FFP aus der Apherese 169,1 mmol/l, also praktisch der gleiche Wert.
Für einen Patienten von 75 kg KG mit einem ECV von 15 l bedeutet dies, dass schon 1 Liter Plasma (ca. 3 FFP) zu einer Erhöhung der Konzentration von fast 2 mmol/l (1,8) isoliertes Natrium führen. Da die im Rahmen eines akuten Volumen-Mangel-Schocks zugeführten FFP-Volumina ein Vielfaches ausmachen können, kann das isolierte Natrium im klinisch relevanten Bereich erhöht werden.
Isolierte Hypernatriämie nach Zufuhr von NaHCO3
Da eine isolierte Hypernatriämie auch als Folge einer Therapie mit Natrium-Bikarbonat zu erwarten ist, das Natrium bleibt zurück während das CO2, aus HCO3 und H+ entstanden, über die Lunge bzw. Niere eliminiert wird, soll die Diskussion dieses Aspekts mit folgenden zwei Beispielen quantifiziert werden.
- Englische Autoren [2] haben nachgewiesen, dass bei der Verwendung von Brausetabletten ganz erhebliche Na-Konzentrationen im Plasma bzw. ECV entstehen können: In ihrer Publikation wird bei Paracetamol bei einer maximalen täglichen Dosis von 500 mg eine Natrium-Konzentration von 148,8 mmol/d genannt (dort Tab. 1). Dies stimmt gut mit den Angaben der deutschen Fachinformation für Paracetamol überein: Bikarbonat (und Spuren von Saccharin) liefern 416 mg Na in 500 mg, bei einer maximalen tägl. Dosis für Erwachsene von 4.000 mg, sind dies 3.328 mg Na pro Tag = 144,6 mmol/d, die im ECV eine Konzentration von 9,6 mmol/d erzeugen, eine erhebliche Erhöhung der Natrium-Konzentration im Sinne von isoliertem Natrium.
- Wird eine typische Lösung von 4,2 % Natriumhydrogencarbonat zur Korrektur metabolischer Acidosen eingesetzt, dann wären dies z.B. beim BE von -10 mmol/l immerhin 400 mmol/l im ECV bzw. Plasma mit der Folge, dass +9,3 mmol/l Bikarbonat und Natrium im ECV erscheinen, und zwar wieder isoliertes Natrium ohne Chloridanstieg [(15 x 142) + (0,4 x 500) = 15,4 x 151,3 mmol/l].
Isolierte Hypernatriämie nach Antibiotika-Therapie
Die gleichen Überlegungen gelten vermutlich für die als Natrium-Salze zugeführten Antibiotika, bei denen das Antibiotikum-Anion im Intrazellularvolumen (ICV) seine Wirkung erzielt und das Natrium (Kation) im Extrazellularvolumen (ECV) zurücklässt.
Im Folgenden werden zwei Tabellen vorgestellt, eine für diejenigen Antibiotika, die als Natrium-Salz geliefert werden und somit im Verdacht stehen, eine isolierte Hypernatriämie zu verursachen, die andere für Antibiotika ohne das entsprechende Kation Natrium. Hier können allerdings andere Natriumsalze enthalten sein, die es auch zu diskutieren gilt.
Tabelle 1
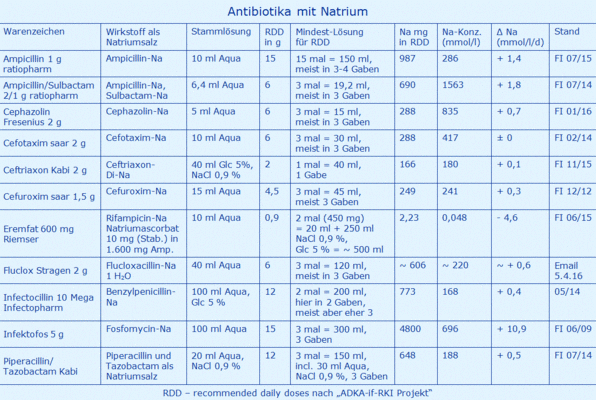
Tabelle 1 ist wie folgt aufgebaut (von links nach rechts): Dem Warenzeichen und Wirkstoff als Natriumsalz folgt die Stammlösung, die RDD und die Angabe, wie oft die Stammlösung zu applizieren ist, um die RDD zu erreichen. Dann folgt die Mindestlösung für die RDD, hier wurde das kleinste mögliche Volumen gewählt, weil für diesen Fall eine potentielle Natrium-Erhöhung am größten ist. Dann folgt der Natriumbetrag in mg für eine RDD und umgerechnet in mmol Natrium (nicht aufgeführt) und damit die Natrium-Konzentration der zugeführten Lösung in mmol/l. Mit dieser, auf der Basis der RDD, zugeführten Lösung wird nun der mögliche Anstieg der Na-Konzentration (ΔNa) in mmol/l/d ermittelt, unterstellt dass der Patient mit 75 kg KG ein ECV von 15 l besitzt und das Natrium in diesem Zeitraum das ECV nicht verlässt.
Der letzte Schritt wird am Beispiel der ersten Zeile der Tabelle (Ampicillin 1 g ratiopharm) beispielhaft beschrieben: (15 l x 142 mmol/l) + (0,15 l x 286 mmol/l) = 15,15 l x 143,4 mmol/l, ergo + 1,4 mmol/l/d.
In der letzten Spalte wird die Quelle für die Angaben benannt, meistens die Fachinformation (FI) des Herstellers oder eine Nachfrage dort per Email.
Die Angaben RDD – recommended daily doses stammen aus dem „ADKA-if-RKI-Projekt [1].
Um eine Stellungnahme gebeten antwortet die Fa. InfectoPharm Arzneimittel Heppenheim (17.06.16): „Aufgrund des Natriumgehaltes von Infectofos sind bei den empfohlenen Dosierungen die Serumelektrolyte zu kontrollieren. Dies ist besonders zu beachten z. B. bei Patienten mit Herzinsuffizienz, Ödemneigung oder sekundärem Hyperaldosteronismus. Ferner sollte der durch Fosfomycin-Gabe bedingte Natriumeintrag in der Elektrolyt- und Wasserbilanz von behandelten Patienten berücksichtigt werden.“
Tabelle 2
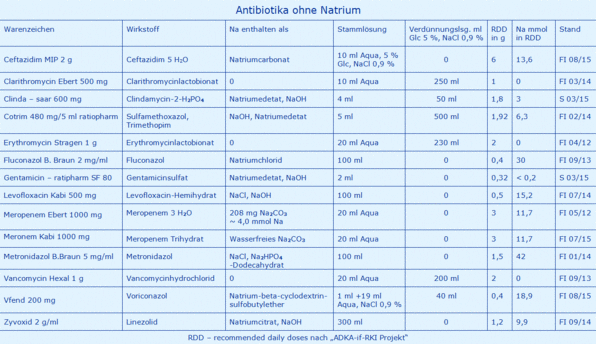
Tabelle 2 ist prinzipiell wie Tabelle 1 aufgebaut, allerdings wurde auf die Berechnung eines möglichen Anstiegs der Na-Konzentration verzichtet, weil das Antibiotikum als Kation kein Natrium enthält.
Stattdessen werden die zusätzlichen Natrium-Quellen wie folgt kommentiert: Es ist fraglich, ob Natrium-Hydrogen-Carbonat oder -Carbonat ein isoliertes Natrium liefert, d.h. ob das Hydrogen-Carbonat oder -Carbonat den Organismus in Form von CO2 + H2O verlässt.
Dies wäre nur dann zu vermuten, wenn der Patient keinen ausgeglichenen Säure-Basen-Status hätte. Allerdings sind die Konzentrationen beim Ceftazidim mit 13,6 mmmol in 10 ml bzw. beim Meropenem mit 11,7 mmol in 20 ml so gering, dass die Natrium-Konzentration im ECV von 15 l nur um maximal 0,6 bis 0,8 mmol/l/d erhöht würde, was als vernachlässigbar klein einzustufen sein dürfte.
Problematik der isolierten Hypernatriämie
Da die Niere nur elektroneutrale Substanzen, also Kation plus Anion, ausscheiden kann, bereitet die iatrogene Zufuhr von Natrium-Azetat, als Beispiel, der Niere Probleme, weil sie für das metabolisierte (CO2 + H2O) Anion ein „neues“ suchen muss, um das Natrium auszuscheiden. Diese Problematik fällt für das Tri-Natrium-Citrat besonders drastisch aus, weil ein besonders großer Anfall von Natrium zu bewältigen wäre. Wie die Niere dieses Problem löst, bleibt vorläufig offen.
Vergleichbar stellt sich die Problematik bei der Therapie der Hypokaliämie dar:
Bei der Zufuhr von Kalium-Chlorid, -Laktat, -Azetat oder Di-Kalium-Aspartat besteht die Erwartung, dass das Kalium-Kation zusammen mit dem Anion in den Intrazellularraum eintritt, um dort die im ECV diagnostizierte Hypokaliämie zu beheben.
Für den Fall des Kalium-Chlorids darf aber vermutet werden, dass das Chlorid nicht in den Intrazellularraum eintritt (Chlorid als idealer Marker des ECV). Für die Niere bedeutet dies eine isolierte Hyperchlorämie, die zu beheben schwierig sein dürfte. Soll die Ausscheidung des Chlorids als Natrium-Chlorid erfolgen, mit der Folge einer isolierten Hyponatriämie?
Klinik der Hypernatriämie
Die Klinik sowohl der einfachen als auch der isolierten Hypernatriämie soll nur mit einer einzigen Abbildung demonstriert werden, die bereits an anderer Stelle verwendet wurde.
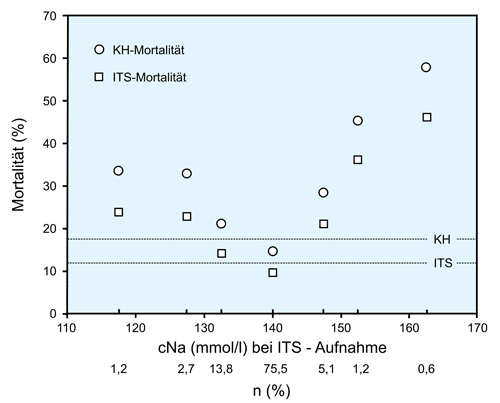
Die Änderung der Natrium-Konzentration scheint ein wichtiger Prognose-Indikator zu sein, wie diese Abbildung verdeutlichen soll: Die Natrium-Konzentration bei Aufnahme (!) auf der Intensivstation (IST) hat offensichtlich einen großen Einfluss auf die Mortalität auf der Intensivstation (IST) bzw. im Krankenhaus (KH). Dies gilt für immerhin 17,7 % der Patienten mit einer Hyponatriämie sowie 6,9 % der Patienten mit einer Hypernatriämie.
Therapie
Die übliche Therapie einer Hypernatriämie mit 5 % Glucose-Lösung wird regelmäßig empfohlen, es muss aber darauf hinwiesen werden, dass diese Therapie mit Vorsicht zu genießen ist, da neben der Na-Senkung auch alle anderen Elektrolyte gesenkt werden, vor allem Kalium betreffend. Da die 5 %ige Glucose-Lösung – zumindest bis zur Einstellung einer normalen Osmolalität – sehr schnell ausgeschieden werden dürfte, könnte der Therapieerfolg möglicherweise nur von kurzer Dauer sein: Wenn normovolämische Probanden innerhalb von ca. 1 Stunde intravenös 1 - 3 l einer 5 %igen Glukose-Lösung erhalten, dann werden davon schon nach 2 Stunden 100 % ausgeschieden [3].
Für den Fall von Infektofos 5 g mit + 10,9 mmol/l/d (Tab. 1) bedeutet dies im Extremfall, dass eine tägliche Erhöhung der Natrium-Konzentration von 142 auf 152,9 mmol/l zu korrigieren wäre, was eine tägliche Zufuhr von 1,1 l einer 5 % Glucose erfordern würde:
15 l x 152,9 + 1,1 l Glucose 5 % = 16,1 l x 142,5 mmol/l.
Die daraus resultierende tägliche Abnahme der Kalium-Konzentration um 0,4 mmol/l (von 4,5 auf 4,1 mmol/l) könnte sich durchaus als Problem erweisen, unterstellt, das Kalium des ICV würde diese Abnahme nicht kompensieren.
Weiterhin sollte der Ausgleich der Natriumkonzentration im Plasma nicht zu rasch erfolgen, damit ein zerebrales Ödem vermieden wird. Vor allem das Gehirn adaptiert an die höhere Natrium-Konzentration, indem die Zellen ihre Natrium-Konzentration ebenfalls leicht anheben. Wird die Flüssigkeit nun zu schnell infundiert, kann es zur Diffusion der intravasalen Flüssigkeit (Wasser) ins Zellinnere kommen, wodurch ein lebensbedrohliches Hirnödem oder andere Hirnschädigungen entstehen können. Eine maximale Reduktion des Plasma-Natriums um 10 mmol//d wird empfohlen.
Fazit
- Einen Sonderfall einer iatrogenen Hypernatriämie stellt die sogenannte isolierte Hypernatriämie dar, primär charakterisiert durch die fehlende Hyperchlorämie.
- Ursächliche Kandidaten für eine isolierte Hypernatriämie sind Natrium-Citrat, -Azetat, -Laktat oder -Aspartat, Natrium-Bikarbonat und das Antibiotika-Natrium.
- Nur im Ausnahmefall können Antibiotika-Präparate zu einer Hypernatriämie führen.
- Die übliche Therapie einer Hypernatriämie mit der 5 %igen Glucose-Lösung ist wegen ihrer Nebenwirkungen, insbesondere der Hypokaliämie, nicht unproblematisch.
Literatur
- ADKA e.V.
Das ADKA-RKI if Projekt für die Surveillance des stationären Antibiotika-Verbrauchs.
Ausschuss Antiinfektive Therapie des Bundesverbands Deutscher Krankenhausapotheker (ADKA e.V.) in Zusammenarbeit mit dem Robert Koch Institut (RKI) - George J, Majeed W, Mackenzie IS, Macdonald TM, Wei L
Association between cardiovascular events and sodium-containing effervescent, dispersible, and soluble drugs: nested case-control study.
BMJ 2013; 26: 347 – 355 - Zander R
Flüssigkeitstherapie, 2. erweiterte (korrigierte) Auflage, 2020
* Co-Autorin
Barbara Reistle
Fachapothekerin für Klinische Pharmazie und Arzneimittelinformation
Marienhospital Stuttgart, Böheimstr.37, 70199 Stuttgart, Vinzenz von Paul Kliniken gGmbH, Stuttgart
barbarareistle(at)vinzenz.de
