
Sauerstoff von A bis Z: Alveole bis Zelle
Konvektion und Diffusion im laufenden Wechsel
Der im oxidativen Stoffwechsel aller Organe und ihrer Zellen laufend verbrauchte Sauerstoff erfordert eine kontinuierliche Nachlieferung, da der Organismus neben dem im Blut vorhandenen O2 über keine größeren O2-Reserven verfügt. Die Nachlieferung erfolgt mit diffusiven und konvektiven Transportprozessen im laufenden Wechsel: Immer dann, wenn Strecken von mehr als wenigen µm zu überwinden sind, mit einer Diffusion von Sauerstoff nicht mehr zu bewältigen, müssen konvektive Transportprozesse eingesetzt werden, nämlich Ventilation und Blutkreislauf (Abb. Transportprozesse).
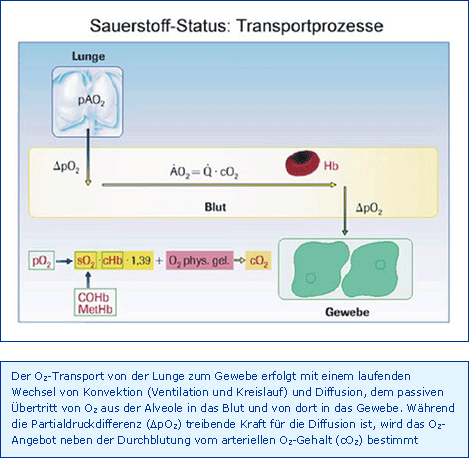
Der Übertritt von O2 von der Alveole in das Blut, ein Weg von wenigen µm, erfolgt durch einfache Diffusion, d. h. die treibende Kraft ist die O2-Partialdruckdifferenz (ΔpO2), also die Differenz zwischen dem alveolären (pAO2) und dem gemischtvenösen O2-Partialdruck (pvO2). Am Ende der physiologischen Oxygenierung bzw. Arterialisierung des Blutes ist die alveolo-arterielle Partialdruckdifferenz (AaDO2) auf wenige mmHg reduziert und damit der arterielle O2-Partialdruck (paO2) fast vollständig an den alveolären angeglichen. Mit dem Kreislauf, einem konvektiven Transport, aufrechterhalten von der Pumpleistung des Herzens, wird der Sauerstoff zu allen Organen und Geweben transportiert. Im Bereich der Mikrozirkulation, die für die Diffusion von O2 vom Blut in das Gewebe mit einer extrem großen Austauschfläche und kurzen Diffusionswegen ausgestattet ist, soll O2 möglichst effektiv alle Gewebezellen erreichen. Wieder ist die O2-Partialdruckdifferenz, dieses Mal zwischen Kapillarblut und Gewebezelle, die treibende Kraft für die Diffusion. Die O2-Versogung des Gewebes ist somit gesichert, wenn eine ausreichend große Menge an Sauerstoff mit dem konvektiven Blutstrom nachgeliefert wird und der O2-Partialdruck, unter dem der Sauerstoff steht, genügend groß ist, einen diffusiven Transport auch zu den entferntesten Gewebezellen zu gewährleisten. Eine Gewebehypoxie, d. h. ein O2-Mangel, kann also ursächlich entweder durch eine Abnahme des konvektiven O2-Transports, der häufigere Fall, oder trotz ausreichender Nachlieferung durch eine Abnahme des kapillären O2-Partialdrucks bedingt sein, der seltenere Fall. Letzterer wäre insofern paradox, als O2 zwar über die Kapillare antransportiert wird, aber ungenutzt am Gewebe vorbeifließt, weil er wegen des zu niedrigen pO2 das Blut nicht verlassen kann (vergl. z. B. CO-Vergiftung).
O2-Utilisation: Bilanz von O2-Angebot und O2-Verbrauch
Unter physiologischen Bedingungen wird immer versucht, das O2-Angebot (AO2) so einzustellen, dass es den O2-Verbrauch (QO2) deutlich übersteigt. Dies gilt gleichermaßen für das O2-Angebot an den Gesamtorganismus wie an die einzelnen Organe. Beide Werte können aus dem Herzzeitvolumen (HZV) oder der regionalen Organdurchblutung (Q) sowie dem arteriellen O2-Gehalt (caO2) wie folgt abgeleitet werden:
AO2 (l/min) = HZV (l/min) x caO2 (l/l)
AO2 (l/min) = Q (l/min) x caO2 (l/l)
Für die Ermittlung des Sauerstoffverbrauchs wird zusätzlich die arteriovenöse O2-Gehaltsdifferenz (avDO2) benötigt, d. h. die Differenz zwischen arteriellem und venösem oder gemischtvenösem O2-Gehalt (cvO2):
QO2 (l/min) = HZV (l/min) x (caO2 - cvO2) (l/l)
QO2 (l/min) = Q (l/min) x (caO2 – cvO2) (l/l)
Für einige lebenswichtige Organe des Menschen sind die Daten des O2-Angebots und des O2-Verbrauchs in Tab. O2-Utilisation zusammengestellt.
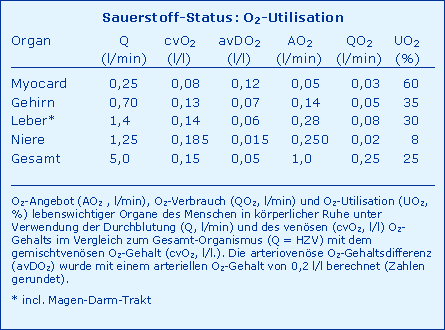
Die für jedes Organ spezifische Bilanz zwischen O2-Verbrauch und O2-Angebot kann über die O2-Utilisation beschrieben werden, d. h. der bezogen auf das Angebot prozentuale Verbrauch bei einmaliger Passage des Blutes durch dieses Organ. Auch diese Daten sind in Tab. O2-Utilisation aufgeführt und demonstrieren folgende Fakten:
Das Organ mit der größten Utilisation ist das Myokard, das Organ mit der kleinsten Utilisation die Niere, die wegen ihrer Ausscheidungsfunktion mit einer extrem großen Durchblutung ausgestattet ist.
Grundsätzlich können alle Organe - mit zwei Ausnahmen bei unterschiedlicher Begründung - den mit dem arteriellen Blut angebotenen Sauerstoff praktisch vollständig utilisieren.
Wegen seiner speziellen O2-Versorgungsbedingungen benötigt das ZNS zumindest zum Erhalt des Bewusstseins einen venösen pO2 von 20 mmHg [Nunn 1993] und die Nieren haben wegen ihrer sehr großen Durchblutung keine Möglichkeit, den angebotenen Sauerstoff zu verbrauchen.
Für alle anderen Organe aber gilt diese Aussage, insbesondere für das Myokard, für das der minimale pvO2 am Menschen mit etwa 5 mmHg bestimmt wurde, und auch für die Leber, die im Tierversuch eine Utilisation von 97 - 100 % erreichen kann. Am Menschen gewonnene Befunde des gemischtvenösen Blutes können als Beleg hierfür dienen: Dialyse-Patienten (keine Nierendurchblutung) mit renaler Anämie (cHb = 10 g/dl) unter maximaler körperlicher Belastung weisen eine sO2 von nur noch 12 % auf, Probanden unter simulierten Höhenbedingungen (4.600 m) bei körperlicher Belastung eine sO2 unter 10 % [Zander 1996 (B)].
O2-Verbrauch oder O2-Aufnahme
Prinzipiell kann der O2-Verbrauch des Menschen auf zwei Wegen bestimmt werden, die unter steady state Bedingungen gleiche Werte ergeben sollten. Einmal der aus Kenntnis des HZV und der avDO2 ermittelte eigentliche O2-Verbrauch QO2 und zum anderen die über die Ventilation, d. h. das Atemzeitvolumen (AZV), zu bestimmende O2-Aufnahme VO2:
VO2 (l/min) = AZV (l/min) x (FIO2 – FEO2)
Bei einem AZV von 7 l/min und einer Differenz der inspiratorischen (FIO2) und exspiratorischen (FEO2) O2-Fraktionen von 0,036 (3,6 %) würde sich wieder der Wert von 0,25 l/min für die VO2 ergeben. Tatsächlich kann diese Übereinstimmung unter klinischen Bedingungen selbst für Pneumonie-Patienten demonstriert werden [Weyland et al. 1994]. Wenn trotzdem je nach eingesetzter Methodik, nämlich respiratorische (offenes bzw. geschlossenes System) oder blutige Verfahren (HZV und avDO2) von einigen Autoren Differenzen zwischen O2-Aufnahme und -Verbrauch beschrieben werden [Nunn 2000], dann dürfte dies am ehesten allein auf methodische Probleme hinweisen.
