
Forum 2 – Citratlösungen
(Ausgabe 03/2011)
Problematik pH
Bereits 2003 [4] wurde nachgewiesen, dass die Aktivität (Aktivierung) wichtiger Gerinnungsfaktoren sehr stark vom pH abhängt: Eine Azidose führt zu einer Senkung, eine Alkalose zu einer Steigerung der Aktivität. Die entsprechenden Befunde sind in der folgenden Abbildung Aktivität der Gerinnungsfaktoren versus pH dargestellt.
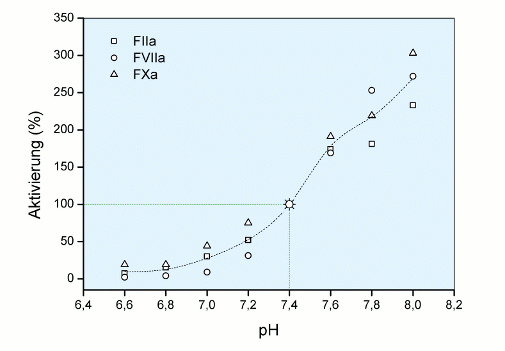
Aus diesen Befunden ist zu schließen, dass der pH-Wert auch die Diagnostik beeinflussen muss. Als logische Konsequenz wurde 2006 unter www.Physioklin.de belegt, dass unter Verwendung gepufferter Reagenzien (Roche Diagnostics) der Einfluss des Patienten-BE auf den Quick-Wert weitgehend „vertuscht“ wird, weil gepufferte Reagenzien die saure Vorgeschichte der Blutprobe aufheben.
Und 2001 wurde auch gezeigt [10], dass sich der pH-Wert einer Blutprobe nach Zugabe von Citrat (9 + 1) erheblich verändert, je nachdem ob gepufferte oder ungepufferte Citratlösungen eingesetzt werden, die Ergebnisse sind in der folgenden Abbildung Plasma-pH versus Citratlösungen wiedergegeben.
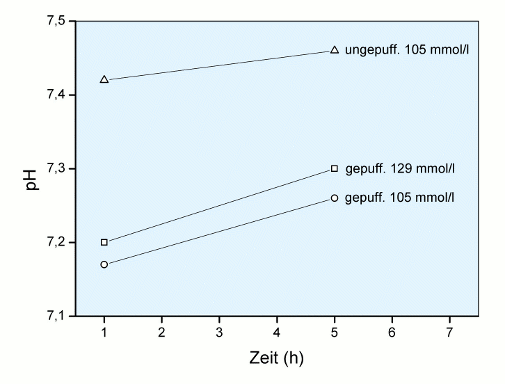
Es ist offensichtlich, dass auch bei gleicher Citrat-Konzentration (105 mmol/l) deutliche pH-Unterschiede auftreten: Eine Pufferung führt zu einer erheblichen Senkung des pH. Aus den Befunden von Töpfer [10] plus Meng [4] können die Konsequenzen einer solchen pH-Senkung abgeleitet werden, wie dies in der Abbildung Aktivität versus Citratlösungen demonstriert wird: Die Gerinnungs-Aktivität wird maßgeblich von der Art der verwendeten Citratlösung bestimmt.
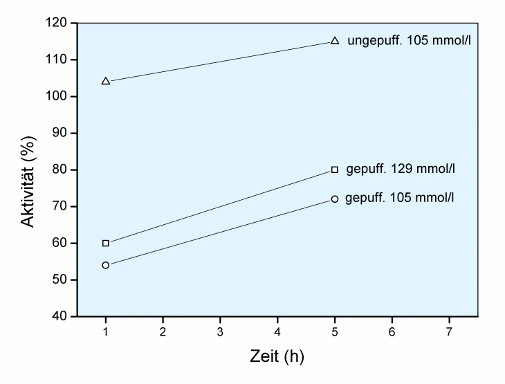
Außerdem fällt auf, dass sich der pH und damit die Aktivität innerhalb von 5 Stunden deutlich nach oben bewegen. Die Autoren [10] betonen, dass die pH-Messung - vorsorglich - aus der Mitte der Plasmaschicht erfolgte, also darf unterstellt werden, dass die pH-Änderung als Folge eines CO2-Verlustes zu interpretieren ist: Je saurer desto deutlicher ausgeprägt, weil der pCO2 dann höher ausfällt, wenn das Bikarbonat des Blutes zuvor mit Citronensäure ausgetrieben wurde.
Fazit 1
Sowohl die im Handel befindlichen Citratlösungen (Präanalytik) als auch die Hersteller-spezifischen Reagenzien (Intraanalytik) bestimmen - über ihren pH-Wert - das spätere Ergebnis der Diagnostik.
Citratlösungen im Handel
Die Konzentrations-Angaben der im Handel befindlichen Citratlösungen wechseln zwischen mol/l bzw. mmol/l und Prozent, dort nicht weiter spezifiziert, meistens unterstellt als % (w/v). Die Angabe in mmol/l ist prinzipiell der in % (w/v) oder % (w/w) vorzuziehen. Weil die Kenntnisse über die Einwaage von Substanzen, d. h. Molekulargewicht plus Hydratwasser, und Prozentangaben, d. h. Gewicht pro Volumen (% (w/v) oder Gewicht pro Gewicht % (w/w) ), leider heute verloren gegangen sind, wird dieser Aspekt im Anhang 1 beschrieben.
Anhand des Beispiels "3,2 %ige Natrium-Citratlösung" soll dies verdeutlicht werden (gleiche Dichte von 1,019 g/ml unterstellt):

Hier ist offensichtlich mehr Präzision gefordert.
Als Beleg für die Problematik werden folgende Literaturangaben genannt:
Die Angabe [5]: "In Deutschland wird überwiegend 0,105 mmol/l (3,2 %) Natriumzitrat verwendet", ist mehrfach falsch: Gemeint ist 105 mmol/l und eine 3,2 %ige (w/v unterstellt) Lösung kann nicht 105 mmol/l enthalten, entweder 3,2 % Tri-Natrium-Citrat ⋅ 2 H2O = 109 mmol/l oder 3,1 % der gleichen Substanz = 105 mmol/l. Weitere Ausführungen dort [5]: Wenn "in den USA eine Lösung mit 0,129 mmol/l (3,8%) verwendet wird, mit Zitronensäure auf pH 5,5 gepuffert", dann ist dies mehrfach falsch und zusätzlich verwirrend: Gemeint ist 129 mmol/l und die Angabe 3,8 % (w/v unterstellt) kann jetzt nicht mehr verwendet werden, weil zwei Substanzen vorliegen. Verwirrend, weil sich die Angabe 129 mmol/l auf die Gesamt-Citrat-Konzentration bezieht, die sich (s. u.) aus 110,3 mmol/l Citrat + 18,9 mmol/l Citronensäure = 129,2 mmol/l Gesamt-Citrat zusammensetzt, ein Puffersystem mit einem pH von angeblich 5,5 (Temperatur?).
An anderer Stelle [2] finden sich die gleichen verwirrenden Angaben: "Röhrchen mit 3,8 % Natriumzitrat (129 mmol/l) und auch mit 3,2 % (105-109 mmol/l) werden im Handel angeboten." Dazu weiter "WHO und NCCLS empfehlen generell 3,2%iges Natriumzitrat für alle Gerinnungsuntersuchungen…" und weiter "grundsätzlich sollte auf pH 5,1 bis 5,3 gepuffertes Zitrat verwendet werden…" und schließlich "das Plasma sollte bei pH 7,3-7,45 gehalten werden ….": Bei welcher Temperatur?
Ähnlich an anderer Stelle [6]: "Der empfohlene Konzentrationsbereich ist 0,105-0,109 mol/l (üblicherweise 3,2 %), das 0,129 molare Citrat (3,8 %) sollte aufgegeben werden, weil seine Citratkonzentration den Sensitivitätsindex (ISI) einiger Thromboplastine modifiziert. Das Citrat muss mit Citronensäure auf einen pH von 5,1-5,3 gepuffert werden, um den pH der Plasmaprobe zwischen 7,3 und 7,45 zu halten.": Bei welcher Temperatur?
Schließlich verwirrt auch ein Hersteller [1] den Anwender: "Das Clinical Laboratory and Standard Institute (vormals NCCLS) empfiehlt, dass das Antikoagulans für Gerinnungstests in einer Konzentration zwischen 0,105 und 0,109 mol/l Trinatriumzitrat vorliegen sollte, was einer 3,2%-igen Zitratlösung entspricht. Die Internationale Gesellschaft für Thrombose und Hämostase (ISTH) empfiehlt eine Konzentration von 0,109 mol/l Zitrat." Eine 3,2%ige Lösung (w/w oder w/v?) kann nicht "zwischen 0,105 und 0,109 mol/l" enthalten, keine Rede mehr von einer Citrat-Citronensäure-Lösung oder einer "gepufferten Citratlösung".
Dagegen das Originalzitat aus Approved Guideline des Clinical and Laboratory Standards Institute (Collection, Transport, and Processing of Blood Specimens for Testing Plasma-Based Coagulation Assays and Molecular Hemostasis Assays, 5th ed. H21-A5; 2008): Das für Gerinnungstests empfohlene Antikoagulans sollte 105-109 mmol/l, 3,13 % bis 3,2 % (üblicherweise als 3,2 % bezeichnet) des Dihydrats von Tri-Natrium-Citrat (Na3C6H5O7 ⋅ 2 H2O) enthalten, gepuffert oder nicht gepuffert. Der letzte Zusatz ist wenig hilfreich, die Spezifizierung von % fehlt auch hier.
Fazit 2
Wissenschaftler, Fachgesellschaften und Hersteller sorgen für Verwirrung, trotzdem sollen zwei der am meisten verbreiteten Lösungen für die In vitro-Gerinnungshemmung versuchsweise definiert werden:
- Citratlösung 109 mmol/l, pH ca. 8,3 (37 °C), hergestellt aus 3,21 % (w/v) Tri-Natrium-Citrat-Dihydrat.
- Citrat-Citronensäure-Lösung 109 mmol/l Citrat, mit 85,5 mmol/l Tri-Natriumcitrat (MW 294,1) plus 23,4 mmol/l Citronensäure, pH = 5,6 (37°C), hergestellt aus 2,515 % (w/v) Tri-Natriumcitrat-Dihydrat plus 0,492 % (w/v) Citronensäure-Monohydrat (MW 210,1).
Blutentnahme-Systeme im Handel

Kommentar [nach 11]: Unterschiedliche Blutentnahme-Systeme, Vacutainer (BD), S-Monovette (Sarstedt) und Venosafe (Terumo), also Faktoren der Präanalytik, führen zu unterschiedlichen Ergebnissen bei der Bestimmung der Prothrombinzeit (PT), diese Unterschiede können durch verschiedene Reagenzien, also Faktoren der Intranalytik, noch verstärkt, aber auch aufgehoben werden.
POC-Geräte im Handel

Verfahren des Zentrallabors und manuelle Verfahren
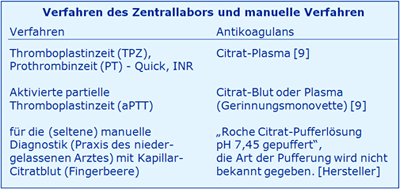
Fazit 3
Im Markt herrscht Verwirrung darüber, welche Citratlösungen zum Einsatz kommen bzw. kommen sollten, dies betrifft die Konzentration und eine mögliche Pufferung. Die Anbieter von Blutentnahmesystemen, also Präanalytik, und die Anbieter von Verfahren und Geräten zur Gerinnungsdiagnostik, also Intraanalytik, scheinen die Brisanz dieser Verwirrung nicht zur Kenntnis zu nehmen.
Warnhinweise zur Präanalytik
Willkürliche Auswahl von Warnungen und Hinweisen zur Präanalytik, mit jeweils einem Kommentar (K) zu möglichen pH-Änderungen.
BD (Vacutainer) [Homepage]:
- Die Prothrombinzeit (PT) und die aktivierte partielle Thromboplastinzeit (APTT) liegen typischerweise bei Proben mit 3,8%igem Zitrat höher als bei Proben mit 3,2%igem Zitrat.
K: Die Konzentration des gepufferten Citrats, d. h. die unterschiedliche Pufferkapazität, beeinflusst den resultierenden pH und damit das Ergebnis. - Patienten, die orale Antikoagulanzien als Therapie erhalten, haben signifikant höhere INR-Werte in 3,8%-igen als in 3,2%-igen Zitratproben.
K: Hier treffen sich Diagnostika und Therapeutika in einem heiklen Bereich, weil die Umrechnung von Quick (%) auf die INR (International Normalized Ratio) vom verwendeten Thromboplastin abhängt [9], das nicht oder unterschiedlich gepuffert ist, was nachweislich den Quick-Wert zusätzlich intraanalytisch beeinflusst.
Greiner (Vacuette) [Homepage]:
- Die Konzentration des Zusatzes im Röhrchen ist exakt auf die Nennfüllmenge abgestimmt. Nur wenn die korrekte Blutmenge abgenommen wird, kann der Zusatz seine vorgesehene Wirkung erzielen.
K: Je nach Blut/Citrat-Verhältnis wirkt sich die gepufferte Lösung unterschiedlich auf den resultierenden pH und damit auf das Ergebnis aus (s. u. Volumenverhältnis).
Inst. für Laboratoriumsmedizin und Pathobiochemie der Charité Berlin [Homepage]:
- Für Untersuchungen der plasmatischen Gerinnung ist ausschließlich eine 3,2% Natriumcitratlösung zu verwenden, für den PFA 100 ausschließlich eine 3,8% Natriumcitratlösung.
K: Offensichtlich hat dieses Institut eigene Erfahrungen gesammelt, eine Angabe über eine Pufferung der Lösungen fehlt. - Die Blutprobe muss sofort nach der Abnahme vorsichtig durch 4-5-maliges Überkopf-schwenken gemischt werden, dabei ist Schaumbildung zu vermeiden.
K: Ein Entweichen von CO2, gefördert durch Schütteln, oder eine Oberflächenvergrößerung infolge Schaumbildung, führt zu einem Anstieg des pH-Wertes und damit Änderung des Ergebnisses. - Bei einem Hk von über 60% müssen die Gerinnungsmonovetten präpariert werden, da durch die geringe Plasmamenge das Plasma/Citrat-Verhältnis zum Citrat verschoben wird.
K: Gemeint ist vermutlich die Tatsache, dass bei einer zu hohen Plasma-Citrat-Konzentration im geringen Plasmavolumen (hoher Hct) die später zugesetzte, definierte Calciumchlorid-Menge das überschüssige Citrat nicht mehr kompensieren kann, ein pH-Effekt ist nicht auszuschließen (s. u. Volumenverhältnis).
Institut für Klinische Chemie des Universitätsklinikums Hamburg-Eppendorf [Homepage]:
- Unterfüllte citrathaltige Monovetten (mehr als minus 10%) werden ausgeschlossen, weil die in den Tests zugesetzte, definierte Calciumchlorid-Menge das überschüssige Citrat nicht mehr ausgleichen kann.
K: Ein pH-Effekt ist nicht auszuschließen (s. u. Volumenverhältnis). - Vor und während des Transports müssen die Blutproben bei Raumtemperatur gehalten werden, sie sollten nicht in den Kühlschrank gestellt werden.
K: Eine Abkühlung auf 4 °C würde den Säure-Basen-Status der Probe massiv verändern, eine Alkalose (pCO2 von ca. 10 mmHg, mit einem pH von ca. 7,8) mit vorübergehender, massiver Gerinnungssteigerung wäre die Folge (inwieweit die Hypothermie-bedingte Gerinnungshemmung diesen Effekt aufheben könnte, kann vorläufig nicht beurteilt werden).
Medizinische Laboratorien Düsseldorf [Homepage]:
- Für den PFA-Test (Thrombozytenfunktionstest) 5 ml Blut in Citrat-Röhrchen (Vacutainer) oder PFA-Spezialröhrchen (Monovette).
K: Eine sinnvolle Vorschrift, unterstellt, dass in beiden Fällen eine gleichwertig gepufferte Citratlösung eingesetzt würde.
Endler et al. 2010 [2]:
- Die Zentrifugation (zur Gewinnung von Plasma) sollte bei Raumtemperatur erfolgen.
K: Eine auf 20 °C abgekühlte Probe weist infolge Löslichkeitserhöhung einen pCO2 von vielleicht 20 mmHg und damit einen pH von vielleicht 7,60 auf, ein atypischer Wert für die Trennung von Plasma und Erythrozyten. - Optimal ist ein Transport ins Labor innerhalb einer Stunde ohne jede starke Agitation der Probe.
K: "Agitation" heißt CO2-Verlust und damit pH-Anstieg.
Volumenverhältnis Citrat/Plasma:
Wiederholt wurde hier darauf hingewiesen, dass das Citrat/Plasma-Volumenverhältnis einen deutlichen Einfluss auf das diagnostische Ergebnis haben kann.
Da in der Literatur vielfach ein möglicher Einfluss von Volumenersatzmitteln (HES, Gelatine) und/oder Änderung des Hämatokrits auf die Blutgerinnung untersucht wurde, wird hier kurz darauf eingegangen.
Wenn beschrieben wird [10], dass bei einem Citrat/Blut-Verhältnis von 1 : 14 eine Hyper- und bei einem Verhältnis von 1 : 9 eine Hypokoagulabilität nachgewiesen werden kann, dann darf vermutet werden, dass neben dem schon erwähnten Citrat/Calcium-Verhältnis weitere Faktoren für diese - vermeintlichen - Gerinnungseffekte von HES oder Gelatine verantwortlich sein können: Eine Dilutionsazidose und eine pH-Verschiebung infolge Abnahme der Pufferkapazität des Blutes infolge Hct-Abnahme, je nachdem, ob gepufferte oder ungepufferte Citratlösungen eingesetzt werden.
Fazit 4
Warnungen und Hinweise zur Präanalytik sind zahlreich vorhanden, in vielen Fällen dürften sie durch bisher nicht berücksichtigte pH-Effekte zu interpretieren sein. Würden Blut- oder Plasmaproben ähnlich wie solche der Blutgas-Diagnostik behandelt, dürften viele Effekte vermutlich verschwinden.
Generelles Fazit
Ein geringfügig modifiziertes Zitat fasst die Problematik der Citratlösungen zusammen [6]: Die Konzentration, der Typ (gepuffert / ungepuffert), das Volumenverhältnis Citrat/Blut, der pH der Citratlösung und der Hämatokrit sind diejenigen präanalytischen Variablen, die den späteren Gerinnungstest besonders beeinflussen.
Anhang 1: Konzentrationen und Chemikalien
Nach dem Europäischem Arzneibuch (European Pharmacopoeia, Ph. Eur. 2) gibt es für die Konzentrationsangaben in Prozent (%) insgesamt 4 Varianten bezüglich der Wahl von Volumen (v) und Gewicht (w), von denen hier zwei zur Diskussion stehen, nämlich % (w/w), also g/100 g Lösung, und % (w/v), also g/100 ml Lösung, je nach Rezeptur. Die am häufigsten eingesetzten Substanzen sind:
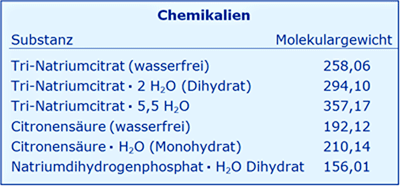
Da gemäß Europäischem Arzneibuch (Eur. Pharm. Monographien 0412 und 0456) Citrat als Dihydrat und Citronensäure als Monohydrat beschrieben werden, kann somit die Prozent-Angabe in mmol/l umgerechnet werden. Beispiel: Die beiden häufig genannten Natriumcitrat-Lösungen 3,13 und 3,8 % enthalten dann die gleiche Konzentration von 108,4 mmol/l, wenn - gewichtsbezogen - die entsprechenden Mengen an 3,13 % (w/w) Tri-Natrium-Citrat ⋅ 2 H2O und 3,8 % (w/w) Tri-Natrium-Citrat ⋅ 5,5 H2O eingewogen werden (Dichte 1,019 g/ml).
Die nach dem Deutschen Arzneibuch (DAB 7) für die Herstellung von Blutpräparaten bekannten Lösungen, also ACD-A und ACD-B, sind ebenso ungenau ohne Angabe des Hydratwassers beschrieben. Allerdings spezifizieren dann die zugehörigen Monographien das Natrium-Citrat als Dihydrat und die Citronensäure als wasserfreie Substanz (ungewöhnlich). Ähnliches gilt für die Britische (BP) Pharmakopoe bezüglich des Natrium-Citrats und die Amerikanische Pharmakopoe (USP) bezüglich der Citronensäure.
Anhang 2: Historische Lösungen [3]
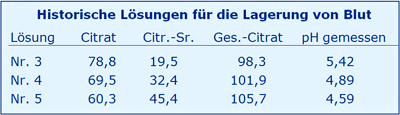
Zur Entwicklung von Lösungen für die Lagerung von Blut wurden folgende Gemische von Citrat und Citronensäure getestet, um im Optimalfalle über einen niedrigen pH (Lösung Nr. 5) die Karamelisierung der Glucose zu verhindern und die Blut-Lagerung zu optimieren.
Angaben in mmol/l (aus den präzisen Angaben % (w/v) Dihydrat/Monohydrat berechnet):
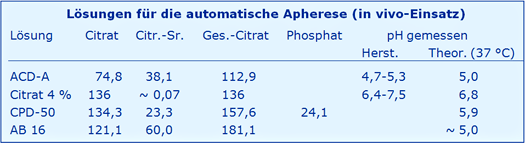
Anhang 3: Automatische Apherese (in vivo-Einsatz)
Von Haemonetics werden hierzu angeboten, alle Angaben in mmol/l aus den präzisen Angaben % (w/v) Dihydrat bzw. Monohydrat berechnet [Hersteller]:
Literatur
- BD (Becton-Dickinson) Blutbild, Ausgabe 13, Mai 2009
- Endler G, Slavka G, Perkmann T, Haushofer A: The importance of preanalytics for the coagulation laboratory. Hämostaseologie 2010; 30: 63-70
- Loutit JF, Mollison PL, Young LM: Citric acid-sodium citrate-glucose mixtures for blood storage. J Exp Physiol 1943; 32: 183-202
- Meng, ZH, Wolberg AS, Monroe DM, Hoffmann M: The effect of temperature and pH on the activity of factor VIIa: Implications for the efficacy of high-dose factor VIIa in hypothermic and acidotic patients. J Trauma 2003; 55: 886 - 891
- Pötzsch B, Madlener K (Hrsg.): Hämostaseologie: Grundlagen, Diagnostik und Therapie. (2. Aufl.), Springer, Berlin-Heidelberg 2010
- Polack B, Schved J-F, Boneu B: Preanalytical recommendations of the ´Groupe d´Etude sur l´hémostase et la thrombose´(GEHT) for venous blood testing in hemostasis laboratories. Haemostasis 2001; 31: 61-68
- Schöler M, Frietsch T: : IAKH-Workshop "Perioperatives Management der Gerinnungsstörung", Workshop 2. Anästh Intensivmed 2007; 48: S134-137
- Schreiner U, Frietsch T, Jámbor C: : IAKH-Workshop "Perioperatives Management der Gerinnungsstörung", Workshop 4 und 5. Anästh Intensivmed 2007; 48: S141-149
- Spiesberger-Heinrich I, Frietsch T, Dorn-Beineke A: IAKH-Workshop "Perioperatives Management der Gerinnungsstörung", Workshop 1. Anästh Intensivmed 2007; 48: S128-133
- Töpfer G, Lutze G, Sauer K et al.: Einfluß der Citratkonzentration im Blutentnahmeröhrchen auf hämostaseologische Meßgrößen. J Lab Med 2001; 25: 162-168
- Van den Besselaar AMHP, Hoekstra MMCL, Witteveen E et al.: Influence of blood collection systems on the prothrombin time and international sensitivity index determinded with human and rabbit thromboplastin reagents. Am J clin Pathol 2007; 127: 724-729
