
Physiologie des arteriellen O2-Status
Die umfassende Beschreibung der O2-Versorgung eines Patienten würde eigentlich die Kenntnis des HZV oder der speziellen Organdurchblutung sowie des arteriellen O2-Gehalts erfordern, also die beiden das O2-Angebot bestimmenden Größen. Da das HZV bzw. die Organdurchblutung nur in Ausnahmefällen bekannt sein dürften, reduziert sich die Beurteilung allein auf den arteriellen O2-Gehalt (synonym O2-Konzentration) bzw. auf die diesen Wert bestimmenden Größen.
Größen des arteriellen O2-Status
Die Größen O2-Partialdruck (pO2, mmHg), O2-Sättigung (sO2, %) und Hämoglobin-Konzentration (synonym Hb-Gehalt) (cHb, g/dl) können zusammen als O2-Status bezeichnet werden. Der Zusammenhang zwischen den einzelnen Determinanten des arteriellen O2-Status ist in Abb. Determinanten dargestellt.
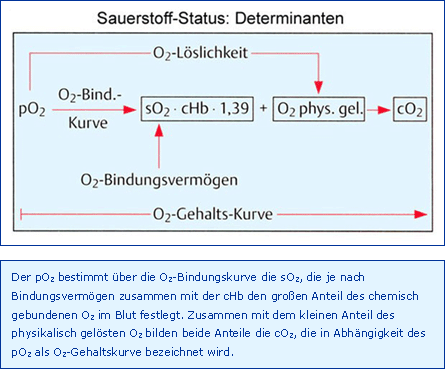
Der arterielle O2-Partialdruck (paO2) zeigt an, ob eine Oxygenation des Blutes während der Passage durch die Lunge erfolgt ist. Er zeigt allerdings nicht an, ob diese O2-Diffusion zu einem physiologischen bzw. ausreichenden O2-Gehalt (caO2) geführt hat. Ein normaler caO2 setzt zwar einen physiologischen paO2 voraus, ein normaler paO2 bewirkt aber nicht automatisch einen physiologischen caO2. Der paO2 bestimmt über die sogenannte O2-Bindungskurve die zugehörige O2-Sättigung des Hämoglobins. Diese sO2 gibt den prozentualen Anteil des oxygenierten Hämoglobins (O2Hb) am Gesamthämoglobin des Blutes an:
sO2 (%) = cO2Hb / (cO2Hb + cHHb + cCOHb + cMetHb) x 100
Bei einer normalen O2-Bindung erreicht sie im arteriellen Blut etwa 96 %. Bei vermindertem O2-Bindungsvermögen hingegen, d. h. bei Anwesenheit von Methämoglobin (MetHb) oder Carboxyhämoglobin (COHb), kann sie nur einen entsprechend kleineren Wert erreichen. Da alle Menschen etwa 0,5 % ihres Hb als MetHb und etwa 0,6 % in Form von COHb vorliegen haben, dürften im arteriellen Blut ca. 3 % des Hb in der desoxygenierten Form (HHb) existieren, was die physiologische sO2 von etwa 96 % erklärt. Aus methodischen Gründen kann neben dieser O2-Sättigung des Hämoglobins - O2Hb als prozentualer Anteil am Gesamt-Hämoglobin - auch eine sogenannte partielle O2-Sättigung definiert werden, wenn der prozentuale Anteil von O2Hb an der Summe von O2Hb plus HHb allein betrachtet werden soll:
psO2 (%) = cO2Hb / (cO2Hb + cHHb) x 100
Partiell wird diese Sättigung genannt, weil nur ein Teil des Hämoglobins, der für den O2-Transport zu Verfügung stehende, betrachtet wird. Die Bezeichnung O2-Sättigung (sO2), bezogen auf Gesamt-Hb, und partielle O2-Sättigung (psO2), bezogen auf OxyHb plus DesoxyHb, wird der Bezeichnung fraktionelle Sättigung oder O2Hb-Fraktion (für sO2) und funktionelle Sättigung (für psO2) vorgezogen. Der Normalwert der psO2 im arteriellen Blut wird mit ca. 98 % angenommen.
O2-Bindungskurve versus O2-Gehaltskurve
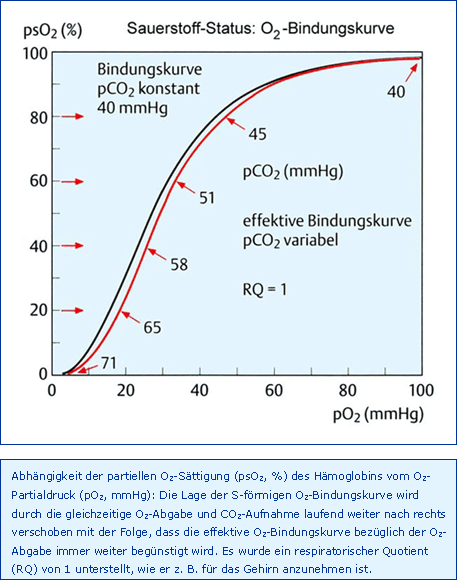
Der Zusammenhang zwischen der O2-Sättigung, und zwar psO2 (%), als Maß für den chemisch gebundenen Sauerstoff, und dem O2-Partialdruck (pO2, mmHg) wird als O2-Bindungskurve bezeichnet (Abb. O2-Bindungskurve). Sie beschreibt nicht nur die O2-Bindung an das Hämoglobin, also die O2-Aufnahme während der Lungenpassage, sondern auch die O2-Abgabe vom Hämoglobin ("O2-Dissoziationskurve"), wie man sie sich für die Mikrozirkulation vorzustellen hätte.
Der klinisch relevantere Zusammenhang, nämlich die O2-Gehaltskurve, also Sauerstoffgehalt (cO2, ml/dl) als Funktion des O2-Partialdrucks (pO2, mmHg), ist in Abb. O2-Gehaltskurve dargestellt.
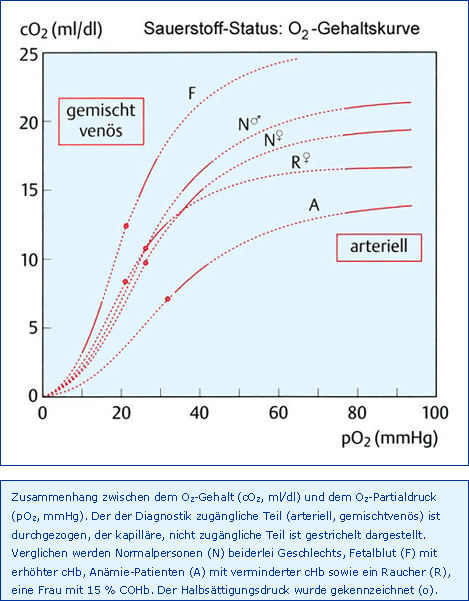
Soll aus der O2-Sättigung (sO2) der Gehalt des chemisch gebundenen O2 berechnet werden, so muss gemäß Abb. Determinanten die cHb mit der sogenannten Hüfner-Zahl multipliziert werden. Letztere gibt die Menge O2 an, die theoretisch maximal (sO2 100 %) an 1 g Hb gebunden werden kann. Ihr Wert wird mit 1,39 ml/g angegeben und kann experimentell nicht überprüft werden, da es kein Verfahren gibt, COHb und MetHb zur Einstellung einer sO2 von 100 % vollständig aus einer Blutprobe zu entfernen. Neben dem großen Anteil von chemisch gebundenem O2 liegt zusätzlich ein kleinerer Anteil von physikalisch gelöstem O2 im Blut vor, der sich mit dem O2-Partialdruck und der O2-Löslichkeit berechnen lässt. Der O2-Gehalt beinhaltet nun die Summe aus chemisch gebundenem und physikalisch gelöstem O2 und wird in ml/dl angegeben. Der Normalwert würde sich bei einer sO2 von 96 %, einer cHb von 15 g/dl und einem Anteil von 0,3 ml/dl physikalisch gelöstem O2 zu 20,3 ml/dl ergeben. Diese O2-Gehaltskurve (s. Abb. O2-Gehaltskurve) allein gestattet die Beschreibung des arteriellen O2-Status sowie die Vorhersage über die Mikrozirkulation, dem Ort der kapillären O2-Abgabe zur Gewebeversorgung. Die O2-Gehaltskurve verdeutlicht besonders gut die beiden physiologischen Anpassungsmechanismen zur Verbesserung des O2-Antransportes zum Gewebe:
- Erhöhung der Hb-Konzentration (O2-Kapazität), hier dargestellt für den Fall des Feten und
- Rechtsverlagerung der O2-Bindungkurve und damit der -Gehaltskurve, hier gezeigt für den Anämie-Patienten.
Zugleich beschreibt sie am Beispiel des Rauchers die unerwünschten Negativeffekte, nämlich
- Linksverlagerung der O2-Bindungskurve und damit der -Gehaltskurve und
- Verminderung der effektiven Hb-Konzentration (O2-Kapazität).
Reversibler O2-Transport durch das Blut
Eine besonders bemerkenswerte Eigenschaft des Blutes besteht darin, dass O2 in der Lunge bereitwillig aufgenommen und trotzdem im Gewebe wieder abgegeben werden kann. Mit anderen Worten: Während das Blut bei der Passage durch die Lungenstrombahn eine möglichst hohe Affinität besitzen sollte, wäre für den Aufenthalt in den Kapillaren der Mikrozirkulation eine möglichst niedrige O2-Affinität erwünscht. Tatsächlich wird das Hämoglobin diesen Anforderungen gerecht, die S-Form mit der Möglichkeit der Lageveränderung (2,3-Diphosphoglycerat, 2,3-DPG) erfüllt diese Ansprüche weitgehend. Eine Konzentrationserhöhung von Stoffwechselmetaboliten im Blut wie H+-Ionen (Milchsäure) und CO2 verursachen eine Rechtsverlagerung der O2-Gehaltskurve, sog. Bohr-Effekt. Die Konsequenzen sind doppelter Natur: Eine systemische Hyperkapnie einerseits führt zu einer problematischen Verschlechterung der O2-Aufnahme in der Lunge und einer Verbesserung der O2-Abgabe an das Gewebe. Eine lokale Aufnahme von CO2 vom Gewebe in das Blut während der Passage durch die Kapillaren des Gewebes andererseits führt zu einer sinnvollen Affinitätsabnahme am Ort der O2-Abgabe. Das Ergebnis, eine sogenannte effektive O2-Bindungskurve, ist zusätzlich in Abb. O2-Bindungskurve dargestellt. Während der Passage des Blutes durch eine Gehirnkapillare, hier wird pro mol abgegebenes O2 auch 1 mol CO2 vom Blut aufgenommen (respiratorischer Quotient 1), wird die O2-Bindungskurve immer weiter nach rechts verlagert. Die Folge davon wäre unter Extrembedingungen, dass bei einer vollständigen Entsättigung des Hämoglobins der zugehörige pO2 immer weiter ansteigt, was die Entsättigung ihrerseits deutlich begünstigen muss. In diesem Falle - effektive O2-Bindungskurve bei lokaler Aufnahme von CO2 - werden zwei positive Effekte miteinander verknüpft. Der klassische, systemische Effektor für die Lage der O2-Bindungs- bzw. -Gehaltskurve ist die intraerythrozytäre 2,3-DPG-Konzentration. Sie reagiert in einigen Stunden in vivo und in vitro auf eine Änderung des pH-Wertes mit der Folge, dass die Rechtsverlagerung bei Azidose über eine Abnahme der 2,3-DPG-Konzentration teilweise aufgehoben wird. Eine über Stunden bestehende Hyperventilationsalkalose, z. B. bei der Höhenanpassung, wird ebenso über die Alkalose bedingte 2,3-DPG-Verminderung teilweise kompensiert.
