
Forum 5 - Intraanalytischer pH-Wert
(Ausgabe 04/2014)
Prinzipielle Vorbemerkungen
Die Tatsache, dass der pH einer Blut- oder Plasma-Probe den Gerinnungsstatus beeinflusst, wird weiterhin von der Fachwelt ignoriert: Im Vergleich zu pH = 7,40 (100 %) beträgt die Gerinnungsaktivität bei pH = 7,20 nur noch ca. 50 % und bei pH = 7,60 immerhin fast 200 % [1].
Daraus ist zu folgern, dass die Gerinnungs-Diagnostik, je nach Verfahren, mit größeren oder kleineren Fehler behaftet ist, wenn der prä- oder intraanalytische pH variiert wird.
Nachdem bereits die präanalytischen pH-Werte von Citratlösungen im Forum 2 sowie eine mögliche Standardisierung des pH im Forum 3 bearbeitet wurden, sollen nun an dieser Stelle die intraanalytischen pH-Werte von plasmatischen Gerinnungstests besprochen werden.
- Die prinzipielle Forderung wird wiederholt: Der ursprüngliche, in vivo-pH-Status der Probe muss unbedingt erhalten bleiben, um auch alle durch Azidose oder Alkalose bedingten Störungen des Gerinnungs-Status diagnostisch zu erfassen und nicht etwa „wegzupuffern“. Beispielsweise muss es möglich sein, die Azidose bedingte, lebensbedrohliche Gerinnungsstörung eines Polytrauma-Patienten zu erfassen und nicht etwa zu negieren.
Experimentelles Vorgehen
Untersucht wurden Reagenzien zur Bestimmung der Prothrombinzeit (PT, TPZ, INR, Quick), der partiellen Prothrombinzeit (PTT, aPTT) und der Fibrinogen-Konzentration der Firmen Instrumentation Laboratory (Kirchheim), Stago (Düsseldorf) und Siemens Healthcare (Eschborn).
Betrachtet werden einerseits Normalblut mit einem Plasma-pH von pH = 7,34 – also venöses Blut (pCO2 = 45 - 50 mmHg), das mit reiner („ungepufferten“) Na3Citrat-Lösung (1 : 10) verdünnt, der pH also nicht schon mit Citronensäure/Citrat verschoben wurde.
Andererseits wird Azidose-Blut mit einem BE von -15 mmol/l und pH = 7,15 untersucht, ebenso „ungepuffert“ vorbehandelt.
In der ersten Untersuchungsreihe wurde wie folgt vorgegangen:
- Der pH und die Pufferkapazität der Reagenzien wurden bei 37 °C bestimmt (Radiometer BMS 2 Mk 2, Kalibrierung mit Präzisions-Phosphatpuffer pH = 6,841 und 7,383). Dazu werden diese vom Ausgangs-pH mit 0,1 M NaOH oder HCl so titriert, dass die Pufferkapazität zwischen pH = 7,20 und 7,60 als Steigung in der Darstellung pH versus zugesetzte Menge NaOH oder HCl (mmol/l) berechnet werden kann. Die Angaben erfolgen in mmol/l/pH.
- Die Vorhersage der pH-Werte im Plasma-Reagenz-Gemisch erfolgt wie folgt.
Die Pufferwirkungen von Plasma und Reagenz werden gemäß ihrer jeweiligen Volumenanteile und gemessenen Pufferkapazitäten ermittelt.
Die Ausgangswerte von Blut mit einer Pufferkapazität von 67,5 mmol/l/pH sind:
a) Normal-Blut mit pH = 7,34, dessen anteiliges, isoliertes Plasma (ohne Zellbestandteile) eine Pufferkapazität von nur noch 63,3 mmol/l/pH hat.
b) Azidose-Blut mit einer Pufferkapazität des Plasmas, die sich (logischerweise) auf 40,6 mmol/l/pH vermindert hat.
Diese Werte wurden dem Siggaard-Andersen-Nomogramm entnommen. Die Mischung muss mit den jeweiligen H+-Konzentrationen berechnet werden, nicht mit den pH-Werten, weil diese ein logarithmisches Maß sind.
In der zweiten Untersuchungsreihe wurde wie folgt vorgegangen:
Frischblut aus der Cubitalvene wurde mit isotoner (106 mmol/l) Na3Citrat-Lösung (1 : 10) entnommen und die Werte für pH und pCO2 zur Kontrolle mit einem GEM 3000 (IL) gemessen (pH = 7,38 bei pCO2 = 40 mmHg, cHCO3 = 23,2 mmol/l). Alle Messungen mit dem GEM 3000 erfolgten im Ansaugmodus („venös“).
Die weiteren Versuche wurden mit dem Serum des gleichen Spenders vorgenommen. Dazu wurde das Blut anstelle von Na3Citrat jetzt 1 : 10 mit 0,9 % NaCl verdünnt, die anschließende Gerinnung abgewartet und danach zentrifugiert. Der für das Serum gemessene pH betrug 7,565 bei einem pCO2 von nur noch 31,5 mmHg (CO2-Verlust mit pH-Anstieg).
In einem Doppelversuch wurde das azidotische Serum mit einem volumetrischen Zusatz von 1 M HCl auf einen Ziel-BE von -12 mmol/l gebracht (pH = 7,15 bei pCO2 = 40 mmHg und cHb = 0 g/dl), dies entspricht einem azidotischen Blut mit einem BE von -15 mmol/l beim Plasma-pH von pH = 7,15 und pCO2 von 40 mmHg (im Folgenden wird das Serum immer als Plasma bezeichnet). Nach Zusatz von HCl lag der resultierende pH <7,0 (Geräteanzeige) bei pCO2 = 147 bzw. 96 mmHg. Mit vorsichtigem Schütteln an der Luft wurde der pCO2 zur „Normalisierung“ schrittweise auf 47 bzw. 40 mmHg gesenkt und damit der pH auf pH = 7,12 bzw. 7,18 angehoben. Der BE betrug dann erwartungsgemäß -12,0 bzw. -11,7 mmol/l.
Die anschließende Verdünnung Plasma : Reagenz beträgt immer 1 : 3, Ausnahme ist nur das Pathrombin SL (Siemens) mit 1 : 2. Bei zwei Verfahren zur PTT (IL und Stago) wird zusätzlich 0,025 M CaCl2-Lösung zugesetzt, ohne dass sich die Verdünnung 1 : 3 ändert.
Bei der Fibrinogen-Bestimmung hingegen beträgt die Verdünnung (nach Hersteller-Empfehlung) 1 : 30, weil das Plasma vor der Reagenzienzugabe (mit 0,9 % NaCl) 1 : 20 vorverdünnt wird und dann die eigentliche Verdünnung 2 : 1 beträgt. Ausnahme ist hier nur das HemosIL Fibrinogen-C (IL), hier beträgt die Verdünnung nur 1 : 15, weil die Vorverdünnung (mit 0,9 % NaCl) nur 1 : 10 beträgt.
Die Plasma-Reagenz-Mischungen erfolgen in Eppendorf Safe-Lock-Gefäßen (1,5 ml), zum Mischen werden die Gefäße nur geschwenkt, um einen CO2-Verlust (pH-Anstieg) zu vermeiden.
Ergebnisse und Interpretation
Alle Ergebnisse sind in der Tabelle wiedergegeben, in der Abbildung das Verhalten des pH im Plasma-Reagenz-Gemisch als Funktion des Reagenz-pH.
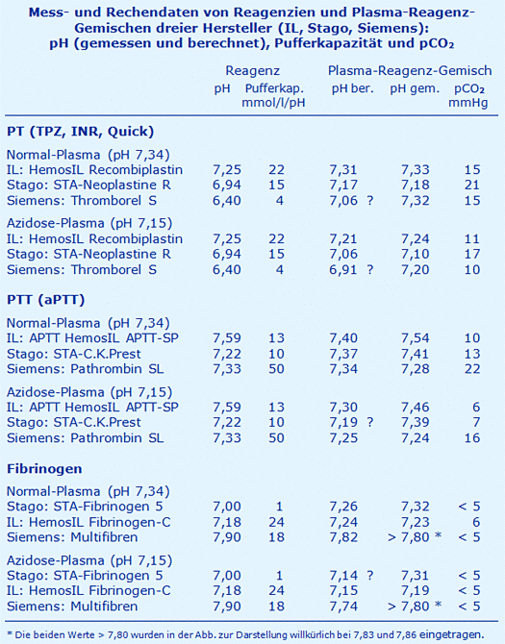
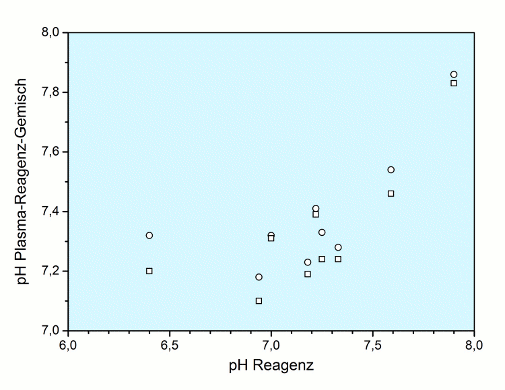
Offensichtlich dominiert der Reagenz-pH den pH des Plasma-Reagenz-Gemisches. Die diagnostisch erwünschten Unterschiede zwischen Normal- (o) und Azidose-Plasma (□) werden in Einzelfällen bei der PTT (Stago: STA-C.K.Prest) und beim Fibrinogen (Stago: STA-Fibrinogen 5) praktisch aufgehoben, während sie in anderen Fällen bei der PT deutlich erhalten bleiben (IL: HemosIL Recombiplastin), und dies sogar in der Nähe des physiologischen pH-Wertes (IL: APTT HemosIL APTT-SP).
Interpretationen
- Die Abweichungen zwischen vorhergesagtem (gemäß Radiometer-pH-Messung und Puffer-Kapazität des Reagenz, ohne CO2, Verdünnung Plasma vs. Reagenz) und gemessenem IL-pH-Wert (mit CO2) sind, abgesehen von 4 (mit Fragezeichen) von 18 Beispielen relativ gering. Die gemessenen IL-pH-Werte liegen tendenziell höher.
- Die Werte des pCO2 mit ihrem Einfluss auf den pH verhalten sich erwartungsgemäß: Der ursprüngliche pCO2-Wert von ca. 45 mmHg (venös 50 mmHg schon 1 : 10 verdünnt) wird durch die Manipulation der Zentrifugation um ca. 12 auf 32 mmHg gesenkt; dann wird er mit der nachfolgenden Verdünnung auf 10 - 20 mmHg weiter verdünnt; bei der Fibrinogen-Bestimmung mit einer Plasma-Verdünnung von 1 : 15 bis 1 : 30 wird dann ein pCO2-Wert von unter 5 mmHg erreicht.
- Die pH-Werte verhalten sich daher entsprechend der Änderung des pCO2:
Wenn die Manipulation der Zentrifugation den pCO2 senkt, muss der pH entsprechend steigen (von ca. pH = 7,40 auf ca. 7,55); wenn der pCO2 sogar auf <5 mmHg fällt, steigt der pH sehr stark auf pH >7,8 an. - Der angestrebte Wert für das azidotische Blut mit BE -15 wird im Plasma mit einem Wert von -12 mmol/l sehr gut getroffen.
- Relativ geringe intraanalytische pH-Unterschiede zwischen den Herstellern finden sich bei der PT, ganz erhebliche pH-Unterschiede allerdings bei der PTT und schließlich beim Fibrinogen mit einem auffallend hohen pH für einen Hersteller (Siemens), was schon allein aus dem hohen pH des Reagenz zu erwarten war.
- Die Pufferkapazitäten der Reagenzien unterscheiden sich erheblich von Reagenz zu Reagenz, wie folgende Beispiele zeigen sollen:
Thromborel S (Siemens) für die PT-Bestimmung mit einer sehr niedrigen, gemessenen Pufferkapazität verändert den vorgegebenen pH der Plasmaprobe sehr wenig (gültig für Normal-und Azidose-Blut) obwohl der Reagenz-pH sehr niedrig ist. Dies wäre als positiv einzustufen.
Bei der PTT hingegen zeigt das Pathrombin SL (Siemens) die höchste Pufferkapazität mit der Folge, dass der resultierende, gemessene pH-Wert von pH = 7,24 bis 7,28 fast unabhängig vom Ausgangs-pH eingestellt wird. Dies wäre als negativ einzustufen, weil die Gerinnungs-relevante Azidose negiert würde.
Die 3 Reagenzien von Stago zeigen im Mittel die niedrigsten Pufferkapazitäten (8,7 mmol/l/pH), gefolgt von den gemittelten IL-Reagenzien (19,7 mmol/l/pH) und Siemens (24 mmol/l/pH), hier allerdings mit einem sehr großen Bereich (4 - 50 mmol/l/pH). - Da die Pufferkapazität des isolierten Plasmas mit 63,3 mmol/l/pH selbst nach Verdünnung mit dem Reagenz (meist 1 : 3) praktisch immer noch größer ist als die des Reagenz nach Verdünnung, spielt die Pufferkapazität in Relation zum pH des Reagenz eine untergeordnete Rolle. Die höchste, gemessene Pufferkapazität (Pathrombin SL, Siemens) liegt bei der vorgegebenen Verdünnung von nur 1 : 2 immer noch unterhalb der von Plasma (25 vs. 31,7 mmol/l/pH).
- Die pH-Werte der Reagenzien haben damit einen größeren Einfluss auf den gemessenen pH-Wert des Plasma-Reagenzien-Gemisches, einen Sonderfall bildet nur Thromborel S (Siemens) mit einem pH-Wert von pH = 6,40. Bei einer Plasma-Verdünnung von 1 : 15 bis 1 : 30 (Fibrinogen) hingegen kehren sich die Verhältnisse um, jetzt beträgt die Pufferkapazität des Plasmas nur noch 2,1 bis 4,2 mmol/l/pH und der pH und die Pufferkapazität des Reagenz dominieren den pH des Gemisches. Im Falle von azidotischem Blut mit einem BE von -15 mmol/l nimmt die Pufferkapazität von 63,3 auf 40,6 mmol/l/pH weiter ab, was natürlich zu einer pH-Dominanz des Reagenz führt. Dieser Effekt ist nicht erwünscht, weil gerade hier die Gefahr besteht, dass der ursprüngliche, für die Diagnostik wichtige pH-Wert des Patienten „weggepuffert“ wird, d. h. die mögliche Azidose-bedingte Gerinnungsstörung wird nicht diagnostiziert.
Fazit
- Offensichtlich gibt es für den pH und die Pufferkapazität der intraanalytischen Reagenzien für die plasmatische Gerinnung keine Standardisierung.
- Der pH der Reagenzien dominiert den pH des Plasma-Reagenzien-Gemisches, er liegt für verschiedene Reagenzien dreier Hersteller zwischen pH = 6,40 und 7,90.
- Die diagnostisch erwünschten pH-Unterschiede in den Plasma-Reagenzien-Gemischen zwischen Normal- (o) und Azidose-Plasma (□) werden je nach Hersteller sehr gut bis gar nicht gewährleistet.
Literatur
Meng, ZH, Wolberg AS, Monroe DM, Hoffmann M
The effect of temperature and pH on the activity of factor VIIa: Implications for the efficacy of high-dose factor VIIa in hypothermic and acidotic patients
J Trauma 2003; 55: 886 – 891
Danksagung
Die Firma Instrumentation Laboratory (Kirchheim) hat freundlicherweise das Gerät GEM 3000 zur Verfügung gestellt.
